题目内容
13.CH4与水蒸气制氢气的反应为CH4(g)+H2O(g)?CO(g)+3H2(g),在2L的密闭容器中,将物质的量各1mol的CH4和H2O(g)混合反应,CH4的平衡转化率与温度、压强的关系如图所示: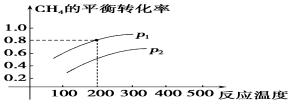
①该反应的△H>0(填“>”或“<”),理由是温度越高,甲烷的转化率越大.
②图中压强p1<p2(填“>”或“<”),理由是反应为气体体积增大的反应,压强越小、转化率越小.
③反应进行到5min时CH4的物质的量为0.5mol,0~5min内的反应速率v(H2)=0.05mol/(L.min).
分析 ①由图可知,相同压强时,温度越高,甲烷的转化率越大;
②由反应可知,减小压强平衡正向移动,由图可知,相同温度时,p1对应的转化率较大;
③结合v=$\frac{△c}{△t}$计算.
解答 解:①由图可知,相同压强时,温度越高,甲烷的转化率越大,可知该反应为吸热反应,升高温度平衡正向移动,△H>0,
故答案为:>;温度越高,甲烷的转化率越大;
②由反应可知,减小压强平衡正向移动,由图可知,相同温度时,p1对应的转化率较大,则p1<p2,即该反应为气体体积增大的反应,压强越小、转化率越小,
故答案为:<;反应为气体体积增大的反应,压强越小、转化率越小;
③2L的密闭容器中,开始时为1mol的CH4,反应进行到5min时CH4的物质的量为0.5mol,0~5min内的反应速率v(H2)=$\frac{△c}{△t}$=$\frac{\frac{1mol-0.5mol}{2L}}{5min}$=0.05mol/(L.min),
故答案为:0.05mol/(L.min).
点评 本题考查化学平衡,为高频考点,把握图中温度、压强对平衡的影响为解答的关键,侧重分析与应用能力的考查,注意反应的特点,题目难度不大.

练习册系列答案
 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案 学习实践园地系列答案
学习实践园地系列答案
相关题目
18.下列说法正确的是( )
| A. | N2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| B. | 某物质在熔融态能导电,则该物质中一定含有离子键 | |
| C. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 | |
| D. | MgF2晶体中的化学键是共价键 |
4.在三个相同体积的密闭容器中分别充入N2、CH4、CO2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
| A. | p(N2)>p(CH4)>p(CO2) | B. | p(CH4)>p(N2)>p(CO2) | C. | p(CH4)>p(CO2)>p(N2) | D. | p(CO2)>p(N2)>p(CH4) |
1.下列叙述中正确的是( )
| A. | 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 | |
| B. | 酸性氧化物一定是非金属氧化物,非金属氧化物不一定是酸性氧化物 | |
| C. | 能够电离出H+的物质一定是酸 | |
| D. | 氧化钠和过氧化钠均能与酸反应生成盐和水,故二者都是碱性氧化物 |
8.类推的思维方法在化学学习和研究中有时会产生错误的结论,因此类比推出的结论最终要经过实践的检验才能决定其正确与否.下列类推结论中正确的是( )
| A. | Cu与Cl2直接化合生成CuCl2;Cu与S直接化合也能得到CuS | |
| B. | Fe3O4可写成FeO•Fe2O3;Pb3O4也可写成PbO•Pb2O3 | |
| C. | Mg失火不能用CO2灭火;Na失火也不能用CO2灭火 | |
| D. | 工业上电解熔融MgCl2制取金属镁;也用电解熔融AlCl3的方法制取金属铝 |
18.根据相关化学概念和原理,下列判断正确的是( )
| A. | 若某反应的生成物总能量低于反应物总能量,则该反应为吸热反应 | |
| B. | 若A2+2D-=2A-+D2,则氧化性:D2>A2 | |
| C. | 若R2-和M+的电子层结构相同,则原子序数:R>M | |
| D. | 若甲、乙两种有机物具有相同的分子式,不同的结构,则甲和乙一定是同分异构体 |
5.下列说法正确的是( )
| A. | 凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物 | |
| B. | 两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体 | |
| C. | 相对分子质量相同的几种化合物,互称为同分异构体 | |
| D. | 组成元素的质量分数相同,且相对分子质量也相同的不同化合物,一定互为同分异构体 |
3.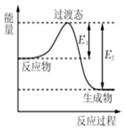 如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)能量变化的示意图,已知E1=xkJ/mol,E2=ykJ/mol,下列有关说法正确的是( )
如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)能量变化的示意图,已知E1=xkJ/mol,E2=ykJ/mol,下列有关说法正确的是( )
 如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)能量变化的示意图,已知E1=xkJ/mol,E2=ykJ/mol,下列有关说法正确的是( )
如图为1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)能量变化的示意图,已知E1=xkJ/mol,E2=ykJ/mol,下列有关说法正确的是( )| A. | 若在反应体系中加入催化剂,E1不变 | |
| B. | 活化能的大小决定了反应热的大小 | |
| C. | 该反应的活化能等于ykJ/mol | |
| D. | 1molSO2Cl2(g)和1molSCl2(g)反应生成SOCl2(g)的△H=(x-y)kJ/mol |