题目内容
14.某主族元素原子R的第五电子层上只有一个电子.下列描述正确的是( )| A. | 其单质在常温下跟水的反应不如钠剧烈 | |
| B. | 其原子半径比钾离子半径小 | |
| C. | In是第5周期ⅠB族元素 | |
| D. | 其氢氧化物能使氢氧化铝溶解 |
分析 由某主族元素R的第五电子层上只有一个电子,根据主族元素的族序数=其最外层电子数,电子层数=周期数,所以该元素属第五周期第ⅠA族,原子序数大于钠钾,化学性质与钠钾相似.同一主族元素,随着原子序数的增大,金属性逐渐增强;原子半径逐渐增大;其最高价氧化物的水化物的碱性逐渐增强,则其氢氧化物能使氢氧化铝溶解,据此进行解答.
解答 解:由某主族元素R的第五电子层上只有一个电子,根据主族元素的族序数=其最外层电子数,电子层数=周期数,所以该元素属第五周期第ⅠA族,原子序数大于钠钾,化学性质与钠钾相似,
A.主族元素由上到下,金属性增强.所以跟水反应比钠剧烈,故A错误;
B.一般情况下,电子层越多,粒子半径越大,该原子含有5个电子层,钾离子含有3个电子层,则其原子半径比钾离子半径大,故B错误;
C.In的原子序数为49,位于第五周期ⅢA族,故C错误;
D.其金属性大于Na,则其氢氧化物碱性大于氢氧化钠,能够使氢氧化铝溶解,故D正确;
故选D.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,明确原子结构与元素周期表的关系为解答关键,注意熟练掌握元素周期表结构、元素周期律内容,试题培养了学生的分析、理解能力及灵活应用能力.

练习册系列答案
相关题目
4.一种熔融碳酸盐燃料电池的工作原理如图所示.下列有关该电池说法正确的是( )
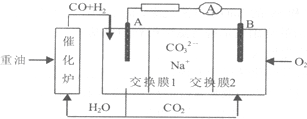

| A. | 重油是石油分馏的产品,含有的主要元素为C、H、O | |
| B. | 电极B上发生的电极反应为:O2+2CO2+4e-═2CO32- | |
| C. | 电极A上H2参与的电极反应为:H2+2OH--2e-═2H2O | |
| D. | 电池工作时,CO32-向电极B移动 |
5.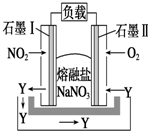 熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
 熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )
熔融盐NaNO3组成的燃料电池如图所示,在使用过程中石墨Ⅰ电极反应生成一种氧化物Y,下列有关说法正确的是( )| A. | 石墨Ⅰ极为正极,石墨Ⅱ极为负极 | |
| B. | Y的化学式可能为NO | |
| C. | 石墨Ⅰ极的电极反应式为NO2+NO${\;}_{3}^{-}$-e-═N2O5 | |
| D. | 石墨Ⅱ极上发生氧化反应 |
9.下列有关有机化合物的性质、结构或用途的说法正确的是( )
| A. | 蛋白质和油脂都属于高分子化合物,一定条件下都能水解 | |
| B. | 乙烯的性质与聚乙烯相同 | |
| C. | 乙醇既可以作燃料,也可以在日常生活中使用,如75%的乙醇经常用于医疗上杀菌、消毒 | |
| D. | 蛋白质溶液中分别加入(NH4)2SO4稀溶液和CuSO4溶液,均有沉淀,原理不相同 |
19.下列化合物,既有离子键也有共价键的是( )
| A. | 氯化氢 | B. | 硫酸 | C. | 氯化铵 | D. | 乙酸 |
6.由A、B、C、D四种金属按下表中装置进行实验.
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙,若电路中转移6.02×1022个e-,则C上增加的质量为3.2g.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活动性由强到弱的顺序是D>A>B>C.
| 装置 | 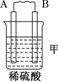 | 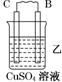 | 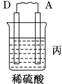 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
(1)装置甲中负极的电极反应式是A-2e-═A2+.
(2)装置乙,若电路中转移6.02×1022个e-,则C上增加的质量为3.2g.
(3)装置丙中溶液的pH变大(填“变大”“变小”或“不变”).
(4)四种金属活动性由强到弱的顺序是D>A>B>C.
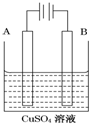 在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答: