题目内容
下列离子方程式中,正确的是( )
| A、将Na2O2固体投入H218O中:2H218O+2Na2O2=4OH-+4Na++18O2↑ |
| B、1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合:2AlO2-+5 H+═Al(OH)3↓+Al3++H2O |
| C、碳酸氢钠溶液与少量氢氧化钡溶液混合:HCO3-+Ba2++OH-=BaCO3↓+H2O |
| D、硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ |
考点:离子方程式的书写
专题:离子反应专题
分析:A.过氧化钠与水的反应中,过氧化钠既是氧化剂,也是还原剂,氧气中的氧元素完全来自过氧化钠,水中氧原子完全转化成氢氧根离子;
B.设溶液体积为1L,偏铝酸钠的物质的量为1mol,氢离子为2.5mol,根据二者物质的量判断过量情况及反应产物;
C.氢氧化钡少量,离子方程式按照氢氧化钡的组成书写,反应产物中碳酸根离子有剩余;
D.醋酸为弱酸,离子方程式中醋酸不能拆开,应该保留分子式.
B.设溶液体积为1L,偏铝酸钠的物质的量为1mol,氢离子为2.5mol,根据二者物质的量判断过量情况及反应产物;
C.氢氧化钡少量,离子方程式按照氢氧化钡的组成书写,反应产物中碳酸根离子有剩余;
D.醋酸为弱酸,离子方程式中醋酸不能拆开,应该保留分子式.
解答:
解:A.将Na2O2固体投入H218O中,水中氧元素完全转化成氢氧根离子,正确的离子方程式为:2H218O+2Na2O2=218OH-+2OH-+4Na++O2↑,故A错误;
B.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合,设溶液体积为1L,溶液中含有1mol偏铝酸根离子、2.5mol氢离子,1mol偏铝酸根离子转化成1mol氢氧化铝沉淀消耗1mol氢离子,剩余的1.5mol氢离子能够溶解0.5mol氢氧化铝,则反应生成的氢氧化铝和铝离子的物质的量相等,反应的离子方程式为:2AlO2-+5 H+═Al(OH)3↓+Al3++H2O,故B正确;
C.碳酸氢钠溶液与少量氢氧化钡溶液混合,反应中碳酸根离子有剩余,正确的离子方程式为:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O,故C错误;
D.硅酸钠溶液与醋酸溶液混合,醋酸不能拆开,正确的离子方程式为:SiO32-+2CH3COOH=H2SiO3↓+2CH3COO-,故D错误;
故选B.
B.1mol/L的NaAlO2溶液和2.5 mol/L的HCl等体积互相均匀混合,设溶液体积为1L,溶液中含有1mol偏铝酸根离子、2.5mol氢离子,1mol偏铝酸根离子转化成1mol氢氧化铝沉淀消耗1mol氢离子,剩余的1.5mol氢离子能够溶解0.5mol氢氧化铝,则反应生成的氢氧化铝和铝离子的物质的量相等,反应的离子方程式为:2AlO2-+5 H+═Al(OH)3↓+Al3++H2O,故B正确;
C.碳酸氢钠溶液与少量氢氧化钡溶液混合,反应中碳酸根离子有剩余,正确的离子方程式为:2HCO3-+Ba2++2OH-=BaCO3↓+CO32-+2H2O,故C错误;
D.硅酸钠溶液与醋酸溶液混合,醋酸不能拆开,正确的离子方程式为:SiO32-+2CH3COOH=H2SiO3↓+2CH3COO-,故D错误;
故选B.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,选项B为易错点,注意根据反应物过量情况正确判断反应产物.

练习册系列答案
相关题目
某合作学习小组讨论辨析:①生活中使用的漂白粉和肥皂都是混合物;②碳酸钠、氢氧化钡、氯化铵、过氧化钠都属于离子化合物;③蔗糖、硝酸钾和硫酸钡分别属于非电解质、强电解质和弱电解质;④醋酸、烧碱、纯碱和生石灰分别属于酸、碱、盐和氧化物;⑤水玻璃、有色玻璃和果冻都是胶体;⑥汽油属于混合物,而液氯、冰醋酸均属于纯净物;⑦烟、雾、豆浆都是胶体.上述说法正确的是( )
| A、①②④⑥⑦ | B、③④⑤⑥ |
| C、②④⑤⑦ | D、①②③⑤⑦ |
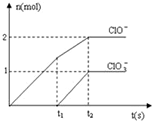 在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、ClO
在一定量的石灰乳中通入一定量的氯气,二者恰好完全反应(发生的反应均为放热反应).生成物中含有Cl-、ClO-、ClO- 3 |
- 3 |
| A、0~t1时,Ca(OH)2与Cl2发生反应的总化学方程式为2Ca(OH)2+2Cl2=Ca(ClO)2+CaCl2+2H2O | ||
B、t2时,Cl-与ClO
| ||
| C、该石灰乳中含有Ca(OH)2的物质的量为10mol | ||
| D、由图可知,生成Ca(ClO3)2的反应是由温度升高引起的 |
在相同温度下,等体积等物质的量浓度的4种稀溶液:①Na2SO4、②H2S、③NaHSO3、④Na2S中所含带电微粒数由多到少的顺序是( )
| A、①=④>③=② |
| B、④=①>③>② |
| C、①>④>③>② |
| D、④>①>③>② |
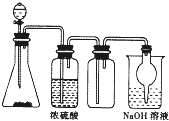 如图是一套实验室制取气体装置,用于发生、干燥、收集和吸收有毒气体,下列各实验能利用这套装置进行的是( )
如图是一套实验室制取气体装置,用于发生、干燥、收集和吸收有毒气体,下列各实验能利用这套装置进行的是( )| A、MnO2和浓盐酸制氯气 |
| B、锌粒和稀硫酸制氢气 |
| C、铜片和浓硝酸制二氧化氮 |
| D、浓氨水和生石灰制氨气 |
向2.5mL 0.2mol/L的Na2CO3溶液中慢慢加入0.1mol/L的盐酸7.5mL,在标况下产生CO2气体的体积是( )
| A、8.4 mL |
| B、5.6 mL |
| C、4.2 mL |
| D、2.8 mL |