题目内容
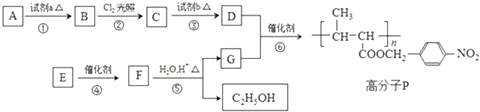
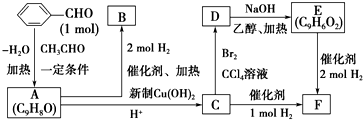
10.A是一种气态烃.B和D是生活中两种常见的有机物.以A为主要原料合成乙酸乙酯,其合成路线如图所示:
(1)A的结构式为
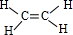
(2)A→B的反应类型为加成反应
(3)D的水溶液与氢氧化钠反应的离子方程式为CH3COOH+OH-=CH3COO-+H2O
(4)B与钠反应的化学方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
(5)写出B→C的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O
(6)写出反应④的化学方程式:
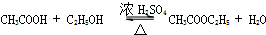 .
.
分析 B和D反应生成乙酸乙酯,B氧化生成C,C氧化生成D,故B为乙醇,C为乙醛,D为乙酸,A与水反应生成乙醇,故A为乙烯,据此解答.
解答 解:B和D反应生成乙酸乙酯,B氧化生成C,C氧化生成D,故B为乙醇,C为乙醛,D为乙酸,A与水反应生成乙醇,故A为乙烯.
(1)A是乙烯,结构式为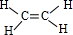 ,故答案为:
,故答案为: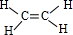 ;
;
(2)A→B是乙烯与水发生加成反应生成乙醇,故答案为:加成反应;
(3)乙酸的水溶液与氢氧化钠反应生成乙酸钠与水,反应离子方程式为:CH3COOH+OH-=CH3COO-+H2O,
故答案为:CH3COOH+OH-=CH3COO-+H2O;
(4)乙醇与钠反应生成乙醇钠与氢气,反应方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
(5)B→C的化学方程式:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(6)反应④是乙醇与乙酸反应生成乙酸乙酯,反应反应方程式为: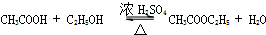 ,
,
故答案为: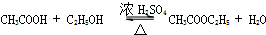 .
.
点评 本题考查有机物的推断,涉及烯烃、醇、醛、羧酸的性质与转化,试题旨在考查学生对有机化学基础的掌握.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
17.下列说法正确的是( )
| A. | 原电池是将电能转化为化学能的装置 | |
| B. | 原电池中发生氧化反应的是负极 | |
| C. | 电解池是将化学能转化为电能的装置 | |
| D. | 电解池中发生氧化反应的是阴极 |
5.下表是元素周期表的一部分.
(1)②、③、④三种元素的原子半径从大到小的顺序是C>N>O(用元素符号表示)
(2)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是NaOH,(填化学式)
(3)表中元素③的氢化物的化学式为NH3,此氢化物的稳定性比元素⑦的氢化物的稳定性强(填“强”或“弱”)
(4)①与②形成的一种化合物是沼气的主要成分,该化合物的电子式为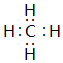
(5)⑥元素最高价氧化物对应的水化物的化学式为Al(OH)3,该物质不能(填“能”或“不能”)溶于氨水,在水中的电离方程式为AlO2-+H++H2O?Al(OH)3?Al3++3OH-.该物质与NaOH溶液反应时的离子方程式为Al(OH)3+OH-=AlO2-+H2O.
(6)⑤、⑥两元素相比较,金属性较强是Na(填元素符号),可以验证该结论的实验是AC
A、比较这两种元素最高价氧化物对应的水化物的碱性
B、比较这两种元素的气态氢化物的稳定性
C、将这两种元素的单质分别放入冷水中
D、比较这两种元素的单质与酸反应时失电子的数目.
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(2)在这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是NaOH,(填化学式)
(3)表中元素③的氢化物的化学式为NH3,此氢化物的稳定性比元素⑦的氢化物的稳定性强(填“强”或“弱”)
(4)①与②形成的一种化合物是沼气的主要成分,该化合物的电子式为
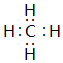
(5)⑥元素最高价氧化物对应的水化物的化学式为Al(OH)3,该物质不能(填“能”或“不能”)溶于氨水,在水中的电离方程式为AlO2-+H++H2O?Al(OH)3?Al3++3OH-.该物质与NaOH溶液反应时的离子方程式为Al(OH)3+OH-=AlO2-+H2O.
(6)⑤、⑥两元素相比较,金属性较强是Na(填元素符号),可以验证该结论的实验是AC
A、比较这两种元素最高价氧化物对应的水化物的碱性
B、比较这两种元素的气态氢化物的稳定性
C、将这两种元素的单质分别放入冷水中
D、比较这两种元素的单质与酸反应时失电子的数目.
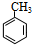
 此烃名称为4-甲基-1-戊炔.
此烃名称为4-甲基-1-戊炔. 的烃可命名为1-甲基-3-乙基苯.
的烃可命名为1-甲基-3-乙基苯. 的烃可命名为:2,4-二甲基-3-乙基戊烷.
的烃可命名为:2,4-二甲基-3-乙基戊烷. 的键线式:
的键线式: .
. 的键线式:
的键线式: .
.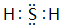 .
.
 .
.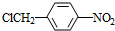 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$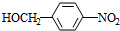 +NaCl.
+NaCl.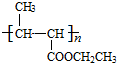 +nH2O$→_{△}^{H+}$
+nH2O$→_{△}^{H+}$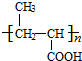 +n CH3CH2OH.
+n CH3CH2OH.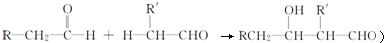 )
)
 、
、 、
、 、
、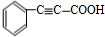 、
、 .
.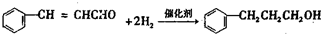 ;
;