题目内容
7.Fe为26号元素,属于第四周期,最外层有2个电子.Fe3+最外层的电子数则为( )| A. | 8 | B. | 13 | C. | 14 | D. | 18 |
分析 铁原子是26号元素的原子,核外电子第分层排布的,每层最多容纳电子数是2n2(n为电子层数),最外层电子数不超过8个,次外层不超过18个,元素铁的原子结构示意图是: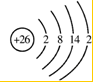 ,铁原子变成铁离子,失去最外层2个电子和次外层上1个电子,由此分析解答.
,铁原子变成铁离子,失去最外层2个电子和次外层上1个电子,由此分析解答.
解答 铁原子是26号元素的原子,核外电子第分层排布的,每层最多容纳电子数是2n2(n为电子层数),最外层电子数不超过8个,次外层不超过18个,元素铁的原子结构示意图是: ,铁原子变成铁离子,失去最外层2个电子和次外层上1个电子,所以铁离子最外层电子数为13,故选B.
,铁原子变成铁离子,失去最外层2个电子和次外层上1个电子,所以铁离子最外层电子数为13,故选B.
点评 本题考查了元素周期表的有关知识,原子变成离子首先失去能量高的电子,比较容易.

练习册系列答案
相关题目
17.下列关于某无色溶液中离子检验的操作、现象与结论对应正确的是( )
| 检验操作 | 现象 | 结论 | |
| A | 加入盐酸酸化的氯化钡 | 产生白色沉淀 | 一定有 SO42- |
| B | 加入氯水与四氯化碳 | 有机层呈紫色 | 一定有 I- |
| C | 加入足量稀盐酸 | 产生无色气体 | 一定有 CO32- |
| D | 加入硝酸银 | 产生白色沉淀 | 一定有 Cl- |
| A. | A | B. | B | C. | C | D. | D |
18.用下列实验装置进行相应实验,能达到实验目的是( )
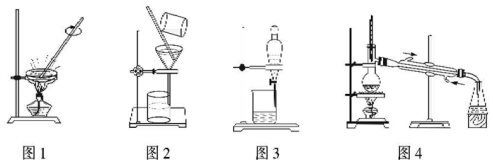

| A. | 用图1所示装置蒸发FeCl3溶液制得无水FeCl3 | |
| B. | 用图2所示装置从Fe(OH)3胶体中过滤出Fe(OH)3胶粒 | |
| C. | 用图3所示装置从CH3OH与C2H5OH的混合物中分离出乙醇 | |
| D. | 用图4所示装置从CH3COOH与CH3COOC2H5的混合物中分离出乙酸乙酯 |
15.对稳定人体血液的pH起重要作用的离子是( )
| A. | Na+ | B. | HCO3- | C. | Fe2+ | D. | Cl- |
2.已知离子反应:Cu2++Zn→Cu+Zn2+,该反应证明Cu2+的氧化性强于( )
| A. | Zn2+ | B. | Zn | C. | Cu | D. | H+ |
12.X、Y、Z、M、W为五种短周期主族元素,X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15;X与Z可形成XZ2分子;Y与M形成的气态化合物溶于水后溶液呈碱性;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 简单的离子半径:W>Z>Y>X | |
| B. | 五种元素中只有X存在同素异形体 | |
| C. | W和M形成的化合物是离子化合物 | |
| D. | 工业上采用电解W和Z形成的化合物制备W单质 |
19.化学与工农业生产、生活密切相关,下列说法中正确的是( )
| A. | 合成纤维和光导纤维都是新型有机非金属材料 | |
| B. | 淀粉、纤维素和油脂都属于天然高分子化合物 | |
| C. | “玉不琢不成器”、“百炼方能成钢”发生的均为化学变化 | |
| D. | 造纸工艺中使用明矾,会导致纸张发生酸性腐蚀,使纸张变脆,易破损 |
16.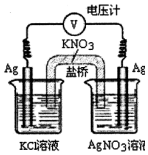 一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
 一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 右池中的银电极作正极 | B. | 总反应为Ag++Cl-═AgCl | ||
| C. | 正极反应为Ag-e-═Ag+ | D. | 盐桥中的NO3-向右池方向移动 |