题目内容
1.实验室用13gZn与稀硫酸反应制取H2(标准状况),请计算:(1)Zn的物质的量;
(2)生成H2的体积.
分析 n(Zn)=$\frac{13g}{65g/mol}$=0.2mol,发生Zn+H2SO4═ZnSO4+H2↑,结合反应及V=nVm计算.
解答 解:(1)n(Zn)=$\frac{13g}{65g/mol}$=0.2mol,答:Zn的物质的量为0.2mol;
(2)由Zn+H2SO4═ZnSO4+H2↑可知,生成气体的物质的量为0.2mol,其体积为0.2mol×22.4L/mol=4.48L,答:生成氢气的体积为4.48L.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应、物质的量关系、体积与物质的量关系等为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | 新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-) | |
| B. | pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) | |
| D. | 0.2mol•L-1CH3COOH溶液与0.1mol•L-1NaOH溶液等体积混合:c(H+)+C(CH3COOH)<C(CH3COO-)+c(OH-) |
12.化学与生产、生活联系密切,下列说法正确的是( )
| A. | 作净水剂的明矾和作消毒剂的漂白粉都是强电解质 | |
| B. | 浸泡过高锰酸钾溶液的硅藻土放于新鲜的水果箱内是为了催熟水果 | |
| C. | 药皂中含有苯酚,能杀菌消毒,故苯酚具有强氧化性 | |
| D. | 合成氨生产中将NH3液化分离,虽可提高N2、H2的转化率但减小了反应速率 |
9.若NA表示阿伏加德罗常数,下列说法中,正确的是( )
| A. | 3mol NO2与足量H2O反应,转移的电子数为NA | |
| B. | 在0℃,101kPa时,22.4 L氢气中含有NA个氢原子 | |
| C. | 25℃,1.01×105Pa,64g SO2中含有的原子数为3 NA | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
16.下列离子在溶液中能大量共存的是( )
| A. | Al3+、Ba2+、OH-、SO42- | B. | Ca2+、H+、Cl-、CO32- | ||
| C. | H+、Ba2+、Ag+、Cl- | D. | K+、OH-、Na+、NO3- |
6.下列实验方法正确的是( )
| A. | 通过测定沸点区别生物柴油和矿物柴油 | |
| B. | 用水区别乙酸、溴苯和硝基苯 | |
| C. | 用溴水区别环己烷、甲苯和环己烯 | |
| D. | 用燃烧法区别乙醇、苯和四氯化碳 |
19.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| B. | 氧的原子结构示意图: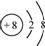 | |
| C. | NaCl的电子式: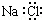 | |
| D. | 质量数为37的氯原子:${\;}_{37}^{17}$Cl |
20.一定能在下列溶液中大量共存的离子组是( )
| A. | 水电离产生的H+浓度为1×10-12 mol•L-1的溶液:Na+、Cl-、HCO3- | |
| B. | 能使pH试纸变深蓝色的溶液:Na+、AlO2-、CO32- | |
| C. | 含有大量Fe3+的溶液:I-、K+、Br- | |
| D. | pH=2的水溶液中:Al3+、NH4+、CH3COO- |