题目内容
FeCl2溶液中混有FeI2杂质,根据已知反应:①2FeCl3+2KI=2FeCl2+2KCl+I2;②2FeCl2+Cl2=2FeCl3;③2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O中的有关事实,要除去其中的FeI2,应选用的试剂是( )
| A、KMnO4 |
| B、过量Cl2 |
| C、FeCl3 |
| D、FeCl2 |
考点:物质的分离、提纯的基本方法选择与应用,氧化性、还原性强弱的比较
专题:元素及其化合物
分析:根据反应中元素化合价的变化来判断氧化剂及氧化性的强弱,再利用氧化性的强弱来分析氧化除去I-而又不影响Fe2+和Cl-.
解答:
解:反应①中Fe元素的化合价降低,则FeCl3为氧化剂,由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性FeCl3>I2,
反应②中Cl元素的化合价降低,则Cl2为氧化剂,由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性Cl2>FeCl3,
反应③中Mn元素的化合价降低,则KMnO4为氧化剂,由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性KMnO4>Cl2,
即氧化性强弱为KMnO4>Cl2>FeCl3,
FeCl2溶液中混有FeI2杂质,要氧化除去I-而又不影响Fe2+和Cl-,
选择氧化性强的物质除杂时能将Fe2+和Cl-氧化,故选择弱氧化剂FeCl3来除杂而不影响Fe2+和Cl-,且没有引入新的杂质,
故选C.
反应②中Cl元素的化合价降低,则Cl2为氧化剂,由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性Cl2>FeCl3,
反应③中Mn元素的化合价降低,则KMnO4为氧化剂,由氧化剂的氧化性大于氧化产物的氧化性可知,氧化性KMnO4>Cl2,
即氧化性强弱为KMnO4>Cl2>FeCl3,
FeCl2溶液中混有FeI2杂质,要氧化除去I-而又不影响Fe2+和Cl-,
选择氧化性强的物质除杂时能将Fe2+和Cl-氧化,故选择弱氧化剂FeCl3来除杂而不影响Fe2+和Cl-,且没有引入新的杂质,
故选C.
点评:本题考查学生利用氧化性的强弱来分析除杂问题,为高频考点,侧重于学生的分析能力的考查,明确氧化还原反应中元素化合价的变化及氧化剂的氧化性大于氧化产物的氧化性是解答本题的关键,难度不大.

练习册系列答案
相关题目
设NA为阿伏伽德罗常数,则下列说法正确的是( )
A、200ml某硫酸盐中含有1.5NA个SO
| ||
| B、一定条件下足量的Fe粉与浓硫酸反应,转移电子数一定为2NA | ||
| C、常温常压下78gNa2O2固体中所含阴、阳离子总数为4NA | ||
| D、电解精炼铜时,若阴极得到电子数为2NA,阳极减少64g |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,46g NO2中含有的分子数为NA |
| B、通常状况下,14g CO含有的电子数目为7NA |
| C、1L 0.2 mol/L的CH3COOH溶液中,H+数目为0.2NA |
| D、0.1mol Cu 和与40mL 10mol/L硝酸反应后,溶液中的NO3-数目为0.2NA |
可逆反应A(g)+3B(g)?2C(g)+2D(g)在4种不同情况下反应速率分别如下,其中反应速率v最大的是( )
| A、v(A)=0.15mol/(L?min) |
| B、v (B)=0.6 mol/(L?min) |
| C、v (C)=0.3 mol/(L?min) |
| D、v (D)=0.1 mol/(L?min) |
以下物质的制备原理错误的是( )
A、2Ag2O
| ||||
B、铝的制备:2Al2O3(熔融)
| ||||
C、工业冶炼铁:4CO+Fe3O4
| ||||
D、无水氯化镁的制备:MgCl2?6H2O
|
类推的思维方式在化学学习与研究中经常采用,但类推出的结论是否正确最终要经过实践的检验.以下类推的结论正确的是( )
| A、Al与S直接化合时可得到Al2S3,则Fe与S直接化合时也可得到Fe2S3 |
| B、CO2通入到硝酸钡溶液中不能生成沉淀,则SO2通入到硝酸钡溶液中也不能生成沉淀 |
| C、乙醛能被银氨溶液氧化,则也能被酸性高锰酸钾溶液氧化 |
| D、Mg(OH)2饱和溶液中c(OH-)=2c(Mg2+),则Al(OH)3饱和溶液中c(OH-)=3c(Al3+) 已知 Ksp[Mg(OH)2]=5.6×10-12,Ksp[Al(OH)3]=2.7×10-32 |
已知2CH3OH(g)?CH3OCH3(g)+H2O(g)△H=-QkJ/mol(Q>0),若某温度下K=400,在1L密闭容器中加入CH3OH,反应到t时刻,各组分浓度如表,判断下列说法正确的是( )
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/mol?L-1 | 0.6 | 1.2 | 1.2 |
| A、此时反应v正<v逆 |
| B、平衡后升高温度,K>400 |
| C、达平衡后再通入H2O(g),甲醇的体积分数一定减小 |
| D、平衡时再加入与起始等量的CH3OH,达新平衡后,CH3OH转化率增大 |
在配制500mL、0.1mol/L的Na2CO3溶液时,下列操作中会导致结果偏高的是( )
| A、将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外 |
| B、定容时俯视刻度线 |
| C、定容时仰视刻度线 |
| D、干净的容量瓶未经干燥就用于配制溶液 |
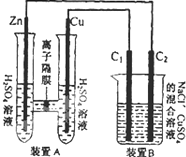 有如图装置,回答下列问题:
有如图装置,回答下列问题: