��Ŀ����
�����½�1molN2��3mol H2 �����Ϊ2L�������л�ϣ��������·�Ӧ��N2��g��+3H2��g��?2NH3��g����2s����NH3���������Ϊ25%��������˵���в���ȷ���ǣ�������
| A����N2Ũ�ȵļ��ٱ�ʾ��ƽ����Ӧ����Ϊ0.2mol?L-1?s-1 |
| B��2sʱN2��ת����Ϊ40% |
| C��2sʱ���������n��N2����n��H2����n��NH3���T3��9��4 |
| D��2sʱNH3��Ũ��Ϊ0.4mol/L |
���㣺��ѧƽ��ļ���
ר�⣺
���������ݻ�ѧƽ������ʽ��ʽ���㣬���������������ͬ������Ϊ�������ʵ����������跴Ӧ�������ʵ���Ϊx
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol�� 1 3 0
�仯����mol�� x 3x 2x
2s����mol�� 1-x 3-3x 2x
2sʱ���NH3���������=
��100%=25%
x=0.4mol��
A����Ӧ����v=
����õ���
B��ת����=
��100%
C���������������жϣ�
D��Ũ��c=
���㣮
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol�� 1 3 0
�仯����mol�� x 3x 2x
2s����mol�� 1-x 3-3x 2x
2sʱ���NH3���������=
| 2x |
| 4-2x |
x=0.4mol��
A����Ӧ����v=
| ��c |
| ��t |
B��ת����=
| ������ |
| ��ʼ�� |
C���������������жϣ�
D��Ũ��c=
| n |
| V |
���
�⣺���������������ͬ������Ϊ�������ʵ����������跴Ӧ�������ʵ���Ϊx
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol�� 1 3 0
�仯����mol�� x 3x 2x
2s����mol�� 1-x 3-3x 2x
2sʱ���NH3���������=
��100%=25%��x=0.4mol��
A����N2Ũ�ȵļ��ٱ�ʾ��ƽ����Ӧ����=
=0.1 mol?L-1?s-1����A����
B��2 sʱN2��ת����=
��100%=40%����B��ȷ��
C��2 sʱ���������n��N2��?n��H2��?n��NH3��=��1-0.4������3-3��0.4����2��0.4=3��9��4����C��ȷ��
D��2 s ʱNH3��Ũ��=
=0.4 mol?L-1����D��ȷ��
��ѡA��
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol�� 1 3 0
�仯����mol�� x 3x 2x
2s����mol�� 1-x 3-3x 2x
2sʱ���NH3���������=
| 2x |
| 4-2x |
A����N2Ũ�ȵļ��ٱ�ʾ��ƽ����Ӧ����=
| ||
| 2s |
B��2 sʱN2��ת����=
| 0.4mol |
| 1mol |
C��2 sʱ���������n��N2��?n��H2��?n��NH3��=��1-0.4������3-3��0.4����2��0.4=3��9��4����C��ȷ��
D��2 s ʱNH3��Ũ��=
| 2��0.4mol |
| 2L |
��ѡA��
���������⿼���˻�ѧƽ�����Ӧ�ã���Ҫ�Ƿ�Ӧ���ʡ�ת���ʡ�Ũ�ȵļ���Ӧ�ã����ջ����ǹؼ�����Ŀ�ϼ�

��ϰ��ϵ�д�
�����Ŀ
X��Y��Z��W����ԭ������������������ֶ���������Ԫ�أ���������������������X��Y��W�ֱ�λ�ڲ�ͬ���ڣ�����Ԫ�����ڱ��У�Z��Y��W�����ڣ���YԪ����ͬ��������Ԫ����δ�ɶԵ�������Ԫ�أ�����˵����ȷ���ǣ�������
| A�����Ӱ뾶��X��Y��Z��W |
| B��Z��W����Ԫ���γɵ����������ƽ�������Σ�Ϊ�Ǽ��Է��� |
| C����X��Y��Z����Ԫ���γɵĻ�����ȿ��������ӻ�����ֿ����ǹ��ۻ����� |
| D��X2Z���۵��X2W�ߣ�����ΪX2Z�����ڴ������ |
ij�������ﺬ�е����ʵ����Ҿ�Ϊ1mol��CuSO4��KCl��NaOH��NH4Cl���ֳɷ��е�ij���֣�ͨ��ʵ��ȷ������ɣ�ȡ������������ˮ���õ���ɫ�������Һ�������Һ�е�����������������Һ�������а�ɫ�������ɣ��ù������������ǣ�������
| A��NaOH��NH4Cl |
| B��KCl��CuSO4 |
| C��KCl��NaOH |
| D��KCl��NH4Cl |
ˮ�ĵ���ƽ��������ͼ��ʾ������˵����ȷ���ǣ�������
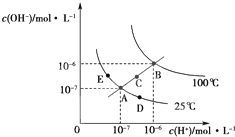

| A��ͼ�����KW��Ĺ�ϵ��B=C=A=D=E |
| B��������B��ʱ����pH=2��������pH=10��KOH��Һ�������ϣ���Һ������ |
| C������A�㵽C�㣬�ɲ��ã��¶Ȳ�����ˮ�м���������NH4Cl���� |
| D������A�㵽D�㣬�ɲ��ã��¶Ȳ�����ˮ�м����������� |
 ���淴Ӧ2X+Y?2Z�ڲ�ͬ�¶ȣ�T1��T2����ѹǿ��P1��P2���£�����Z�����ʵ���n��z���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ���� ��������
���淴Ӧ2X+Y?2Z�ڲ�ͬ�¶ȣ�T1��T2����ѹǿ��P1��P2���£�����Z�����ʵ���n��z���뷴Ӧʱ�䣨t���Ĺ�ϵ��ͼ��ʾ�������ж���ȷ���� ��������| A��T1��T2��P1��P2 |
| B��T1��T2��P1��P2 |
| C��T1��T2��P1��P2 |
| D��T1��T2��P1��P2 |