题目内容
4.碘在不同状态下(固态或气态)与氢气反应的热化学方程式如下所示:①H2(g)+I2(?)═2HI(g);△H=+9.48kJ/mol
②H2(g)+I2(?)═2HI(g);△H=-26.48kJ/mol
下列判断正确的是( )
| A. | ①中的I2为固态,②中的I2为气态 | |
| B. | ②的反应物总能量比①的反应物总能量低 | |
| C. | ①的产物比②的产物热稳定性更好 | |
| D. | 1 mol固态碘升华时将吸热17 kJ |
分析 根据同种物质气态时具有的能量比固态时高,所以等量时反应放出能量高,已知反应①吸收能量,反应②放出能量,所以反应②中碘的能量高,则反应②中碘为气态,据此分析.
解答 解:A.已知反应①吸收能量,反应②放出能量,所以反应②中碘的能量高,则反应②中碘为气态,①中的I2为固态,故A正确;
B.已知反应①吸收能量,反应②放出能量,所以反应②中碘的能量高,所以②的反应物总能量比①的反应物总能量高,故B错误;
C.反应①②的产物都是气态碘化氢,所以二者热稳定性相同,故C错误;
D.根据盖斯定律,②-①为,即I2(s)?I2(g)△H=-35.96KJ,故D错误.
故选A.
点评 本题考查了反应中的能量变化,题目难度不大,注意同种物质气态时能量大于固态.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
15.下列实验现象预测正确的是( )
| A. | 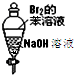 振荡后静置,溶液不再分层,且保持无色透明 | |
| B. |  铁片最终完全溶解,且高锰酸钾溶液变无色 | |
| C. |  微热稀HNO3片刻,溶液中有气泡产生,广口瓶内出现红棕色气体 | |
| D. |  当溶液至红褐色,停止加热,液体变为黄色 |
12.用铝制易拉罐收集满CO2,快速加入过量NaOH浓溶液,立即把口封闭.发现易拉罐“咔咔”作响,并变瘪了;过一会儿,易拉罐又会作响并鼓起来.下列说法正确的是( )
| A. | 导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3- | |
| B. | 导致易拉罐又鼓起来的反应是:Al3++3HCO3-═Al(OH)3+3CO2 | |
| C. | 上述过程中与NaOH溶液反应的物质有三种,且反应结束后的溶液显碱性 | |
| D. | 若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 |
19.鉴别KCl、KBr、KI三种溶液选用的试剂为( )
| A. | CCl4 | B. | AgNO3溶液 | C. | 溴水 | D. | 淀粉溶液 |
9.下列有关叙述正确的是( )
| A. | 加入催化剂会改变反应的焓变 | |
| B. | 已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 | |
| C. | 含20.0g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则该反应中和热的热化学方程式为:NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(aq);△H=-57.4 kJ/mol | |
| D. | 已知C(石墨,s)=C(金刚石,s);△H>0,则金刚石比石墨稳定 |
16.设NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 27 g铝原子最外层电子总数为NA | |
| B. | 2.8 g N2和2.8 g NO2所含电子数均为1.4NA | |
| C. | 1 L 0.1 mol•L-1乙酸溶液中H+数为0.1NA | |
| D. | 标准状况下,22.4 L甲烷的分子数NA |
 .
.