题目内容
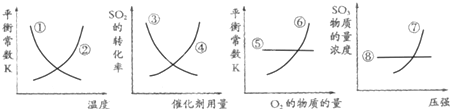
工业上制硫酸的第二步反应:2SO2(g)+O2(g)?2SO3(g)△H<0,反应达到平衡后,改变某一个条件,如图示意图曲线①~⑧中正确的是( )

| A、①⑥⑧ | B、①⑤⑦ |
| C、②③④ | D、③⑥⑦ |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:由于该反应是气体体积减小且放热的反应,所以当温度升高时,平衡逆向移动,平衡常数减小;使用催化剂对平衡移动没有影响,所以反应物转化率不变;平衡常数只受温度的影响,所以增加氧气的物质的量,平衡常数不变;压强增大,平衡向正反应方向移动,所以三氧化硫的物质的量浓度增大,据此判断;
解答:
解:由于该反应是气体体积减小且放热的反应,所以当温度升高时,平衡逆向移动,平衡常数减小;使用催化剂对平衡移动没有影响,所以反应物转化率不变;平衡常数只受温度的影响,所以增加氧气的物质的量,平衡常数不变;压强增大,平衡向正反应方向移动,所以三氧化硫的物质的量浓度增大,所以图中①⑤⑦三条曲线是正确的,故选B;
点评:本题主要考查了外界条件对化学平衡的影响,难度不大,解题时要注意正确分析各个图象.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
下列反应不是氧化还原反应的是( )
| A、HCl+NaOH═NaCl+H2O |
| B、2KClO3═2KCl+3O2↑ |
| C、H2+CuO═Cu+H2O |
| D、2Mg+O2═2MgO |
某两种气态烃组成的混合物,取其2.24L(标准状况下)充分燃烧,得到0.16mol二氧化碳气体和3.6g液态水.据此判断下列分析中不正确的是( )
| A、此气体中一定含有甲烷 |
| B、此混合气体中可能含有乙烷 |
| C、此混合气体中一定不含有丙烷 |
| D、此气体若是乙烯与甲烷的混合气体,则甲烷与乙烯的体积比为2:3 |
下列反应属于加成反应的是( )
A、CH2=CH2+HBr
| |||
B、 +Br2 +Br2
 +HBr +HBr | |||
C、2CH3CH2OH+O2
| |||
D、CH4+2Cl2
|
下列溶液中微粒的物质的量浓度关系不正确的是( )
| A、Ca(ClO)2溶液中:c(ClO-)>c(Ca2+)>c(OH-)>c(H+) |
| B、等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)-c(X-)>c(OH-)>c(H+) |
| C、常温下,将25mL0.2mol/L的盐酸与l00mL0.lmol/L的氨水混合,所得溶液中:c(NH4+)>c(Cl-)>c(NH3?H2O)>c(OH-)>c(H+) |
| D、将0.lmol/L的Na2S溶液与0.lmol/L的NaHS溶液等体积混合,所得溶液中:c(S2-)+2c(OH一)═2c(H+)+c(HS-)+3c(H2S) |
某化合物的结构(键线式)及球棍模型如下.该有机分子的核磁共振波谱图如下(单位是ppm):
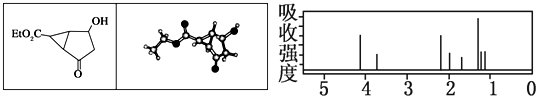
下列关于该有机物的叙述正确的是( )

下列关于该有机物的叙述正确的是( )
| A、右图中最强吸收峰与最弱吸收峰高度比为3:2 |
| B、该有机物分子中含有4个手性碳原子 |
| C、键线式中的Et代表的基团为-CH3 |
| D、该有机物在一定条件下能够发生消去反应和取代反应,但不能发生还原反应 |
能源可划分为一级能源和二级能源,直接来自自然界的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源.氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:2H2O(l)
2H2(g)+O2(g),该反应需要吸收大量的热,下列叙述正确的是( )
| ||
| A、水煤气是二级能源 |
| B、水力是二级能源 |
| C、天然气是二级能源 |
| D、电能是一级能源 |
下列有机物分子在核磁共振氢谱中只给出一种信号的是( )
| A、HCHO |
| B、CH3OH |
| C、HCOOH |
| D、CH3COOCH3 |
