题目内容
在合成氨工业中,实现下列目的变化过程中与平衡移动无关的是( )
| A、为增加NH3的日产量,不断将NH3分离出来 |
| B、为增加NH3的日产量,使用催化剂 |
| C、为增加NH3的日产量,采用500℃左右的高温 |
| D、为增加NH3的日产量,采用2×107-5×107Pa的压强 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:平衡移动原理为:如果改变影响平衡的条件,平衡将向着能够减弱这种改变的方向移动;在使用平衡移动原理时,反应必须是可逆反应且存在平衡移动,否则平衡移动原理不适用.
解答:
解;A.不断将氨分离出来,可以降低生成物的浓度,使平衡向正反应方向移动,从而提高氨的产量,故A不选;
B.使用催化剂,只能同等倍数地增加正、逆反应速率,缩短反应达到平衡所需要的时间,但平衡不发生移动,故B选;
C.采用500℃左右的高温,是因为此温度下,催化剂活性最高,而正反应放热,温度过高不利于平衡向正反应方向移动,故C不选;
D.用高压,使平衡向生成氨的方向移动,有利于氨的生产,与平衡移动有关,故D不选.
故选B.
B.使用催化剂,只能同等倍数地增加正、逆反应速率,缩短反应达到平衡所需要的时间,但平衡不发生移动,故B选;
C.采用500℃左右的高温,是因为此温度下,催化剂活性最高,而正反应放热,温度过高不利于平衡向正反应方向移动,故C不选;
D.用高压,使平衡向生成氨的方向移动,有利于氨的生产,与平衡移动有关,故D不选.
故选B.
点评:本题考查了工业上合成氨的反应,侧重于化学平衡与生成的关系,主要涉及压强、浓度、温度、催化剂对化学平衡的影响,题目难度不大.

练习册系列答案
相关题目
NA代表阿伏加德常数,下列说法中,正确的是( )
| A、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
| B、2 g氢气所含原子数目为NA |
| C、在常温常压下,11.2 L氮气所含的原子数目为NA |
| D、17 g氨气所含电子数目为10 NA |
H2SO3水溶液中存在电离平衡H2SO3?H++HSO3-和HSO3-?H++SO32-,若向H2SO3溶液中( )
| A、通入氯气,溶液中氢离子浓度增大 |
| B、通入过量H2S,反应后溶液pH减小 |
| C、加入氢氧化钠溶液,平衡向右移动,pH变小 |
| D、加入氯化钡溶液,平衡向右移动,会产生亚硫酸钡沉淀 |
达平衡状态的可逆反应:N2(g)+3H2(g)?2NH3(g),改变某一条件,一段时间后,测得正反应速率以N2的浓度减小表示:v(N2)=0.6mol/(L?min),逆反应速率以NH3的浓度减小表示:v(NH3)=1.2mol/(L?min),此时可逆反应的状态是( )
| A、测定时,v正>v逆 |
| B、测定时,v正<v逆 |
| C、测定时,v正=v逆 |
| D、不可能达到新平衡 |
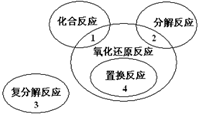 氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于1区的是( )
氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于1区的是( )| A、Cl2+2KBr═Br2+2KCl |
| B、2NaHCO3═Na2CO3+H2O+CO2 |
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 |
| D、2Na2O2+2CO2═2Na2CO3+O2 |
在水中存在H2O?H++OH-平衡,加入下列哪种物质或进行哪项操作,不会使平衡发生移动( )
| A、加入NaOH固体 |
| B、加入NaCl固体 |
| C、加入CH3COOH固体 |
| D、升温 |
25℃时,水的电离达到平衡;H2O?H-+OH-△H>0,下列叙述正确的是( )
| A、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B、向水中加入少量固体硫酸氢钠,c(H-)降低 |
| C、向水中加入少量固体氢氧化钠,平衡正向移动,c(H-)降低 |
| D、将水加热,KW增大,pH不变 |
对于同一周期从左到右的主族元素,下列说法中正确的是( )
| A、原子半径逐渐减小 |
| B、元素的金属性逐渐增强 |
| C、最高正化合价逐渐增大 |
| D、单质的熔沸点逐渐降低 |