题目内容
已知如图中A为单质,D为气体,E和H均为白色沉淀,其中H不溶于稀硝酸,反应中的水和部分产物已略去.
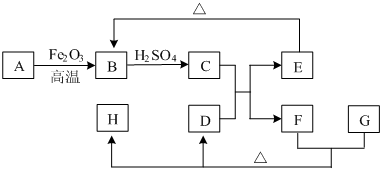
根据框图回答问题:
(1)D的化学式为 .
(2)写出“A→B”发生反应的化学方程式 .
(3)若在C的溶液中逐滴滴加G溶液,生成的沉淀先增多,后减少,分别写出上述过程中发生反应的离子方程式 、 .

根据框图回答问题:
(1)D的化学式为
(2)写出“A→B”发生反应的化学方程式
(3)若在C的溶液中逐滴滴加G溶液,生成的沉淀先增多,后减少,分别写出上述过程中发生反应的离子方程式
分析:B与硫酸反应产物C应为硫酸盐,和气体D反应生成E为白色沉淀,加热可分解生成B,则B应为氧化物,反应A与氧化铁的反应应为铝热反应,则A为Al,B为Al2O3,C为Al2(SO4)3,D应为NH3,E为Al(OH)3,F为(NH4)2SO4,H不溶于硝酸,应为BaSO4,则G为Ba(OH)2,结合对应物质的性质以及题目要求解答该题.
解答:解:B与硫酸反应产物C应为硫酸盐,和气体D反应生成E为白色沉淀,加热可分解生成B,则B应为氧化物,反应A与氧化铁的反应应为铝热反应,则A为Al,B为Al2O3,C为Al2(SO4)3,D应为NH3,E为Al(OH)3,F为(NH4)2SO4,H不溶于硝酸,应为BaSO4,则G为Ba(OH)2,
(1)由以上分析可知D为NH3,故答案为:NH3;
(2)“A→B”发生反应为铝热反应,方程式为2Al+Fe2O3
2Fe+Al2O3,
故答案为:2Al+Fe2O3
2Fe+Al2O3;
(3)在Al2(SO4)3溶液中,逐滴加入Ba(OH)2,首先发生2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓,
当SO42-全部生成BaSO4,继续加入Ba(OH)2,发生Al(OH)3+OH-=AlO2-+2H2O,
故答案为:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓;Al(OH)3+OH-=AlO2-+2H2O.
(1)由以上分析可知D为NH3,故答案为:NH3;
(2)“A→B”发生反应为铝热反应,方程式为2Al+Fe2O3
| ||
故答案为:2Al+Fe2O3
| ||
(3)在Al2(SO4)3溶液中,逐滴加入Ba(OH)2,首先发生2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓,
当SO42-全部生成BaSO4,继续加入Ba(OH)2,发生Al(OH)3+OH-=AlO2-+2H2O,
故答案为:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓;Al(OH)3+OH-=AlO2-+2H2O.
点评:本题考查无机物的推断为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合运用的考查,题目难度中等,注意把握题给信息,结合转化关系进行推断.

练习册系列答案
相关题目

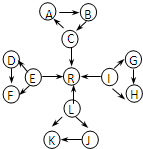 元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):
元素及其化合物是中学化学的主干知识,我们在整理元素化合物之间的相互转化时,发现有些物质间存在如图所示的三角转化关系(部分反应物或生成物已略去):
 (2009?郑州一模)如图表示某典型金属单质A与其化合物之间的转化关系(某些产物和反应条件已略去).已知:图中所示物质中的组成元素均为短周期元素,化合物C中含有两种金属元素,反应⑤用于工业制取A,反应⑥的产物过滤后得到化合物D的溶液呈碱性.
(2009?郑州一模)如图表示某典型金属单质A与其化合物之间的转化关系(某些产物和反应条件已略去).已知:图中所示物质中的组成元素均为短周期元素,化合物C中含有两种金属元素,反应⑤用于工业制取A,反应⑥的产物过滤后得到化合物D的溶液呈碱性.