题目内容
下列实验描述,符合事实的是( )
| A、金属钠暴露在空气中,表面变暗,生成淡黄色固体氧化钠 |
| B、用坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼白光,放出大量的热,产生白色固体 |
| C、用坩埚钳夹住铝箔在酒精灯上点燃,发出耀眼的白光,放出大量的热 |
| D、用坩埚钳夹住铝箔在酒精灯上加热至熔化,轻轻晃动,有液态的铝滴落下来 |
考点:钠的化学性质,镁的化学性质,铝的化学性质
专题:
分析:A.常温下钠表面生成白色固体氧化钠;
B.根据镁在空气燃烧的现象分析;
C.铝箔在空气中不能燃烧;
D.给铝箔在酒精灯上加热时,铝熔化,而形成的氧化铝薄膜熔点高未熔化,包裹着的内层熔化的铝而不会滴落;
B.根据镁在空气燃烧的现象分析;
C.铝箔在空气中不能燃烧;
D.给铝箔在酒精灯上加热时,铝熔化,而形成的氧化铝薄膜熔点高未熔化,包裹着的内层熔化的铝而不会滴落;
解答:
解:A.氧化钠是白色固体,故A错误;
B.坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼的白光,放出大量的热,产生白色氧化镁固体,故B正确;
C.铝箔在空气中不能燃烧,故C错误;
D.用坩埚钳夹住一小块铝箔,由于铝熔点低,所以在酒精灯上加热铝熔化,失去了光泽,由于氧化铝熔点较高,加热时氧化膜包裹着的内层熔化的铝而不会滴落,故D错误;
故选B.
B.坩埚钳夹住打磨过的镁带,在酒精灯上点燃,发出耀眼的白光,放出大量的热,产生白色氧化镁固体,故B正确;
C.铝箔在空气中不能燃烧,故C错误;
D.用坩埚钳夹住一小块铝箔,由于铝熔点低,所以在酒精灯上加热铝熔化,失去了光泽,由于氧化铝熔点较高,加热时氧化膜包裹着的内层熔化的铝而不会滴落,故D错误;
故选B.
点评:本题综合考查元素化合物知识,涉及铝、钠以及镁的性质,为高频考点,侧重于学生的分析能力的考查,注意相关基础知识的积累,题目难度不大.

练习册系列答案
相关题目
下列说法中不正确的是( )
| A、开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径 |
| B、废旧电池不能随意丢弃,要进行深埋处理,防止重金属污染 |
| C、Zn具有还原性和导电性,可用作锌锰干电池的负极材料 |
| D、据测定,许多反应的温度每升高10℃,其反应速率增加2~4倍.在实验室或工业生产中,常采用加热的方法使化学反应在较高的温度下进行,以提高反应速率 |
下列叙述正确的是( )
| A、天然油脂的分子中含有酯基,属于酯类 |
| B、苯的分子式为C6H6,分子中的碳原子远远没有饱和,因此能和氯水发生加成反应 |
| C、所有卤代烃都难溶于水,且都是密度比水大的液体 |
| D、天然气与液化石油气的成分相同,与水煤气的成分不相同 |
下列实验操作合理的是( )
| A、用稀硫酸清洗做焰色反应的铂丝 |
| B、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
| C、用100mL容量瓶配制50mL 0.1 mol?L-1的盐酸 |
| D、测NaOH熔点时可以将NaOH放入石英坩埚中高温熔化 |
同温同压下,下列各组热化学方程式中,△H1<△H2是( )
A、C(s)+
| ||||
B、
| ||||
| C、2H2(g)+O2(g)=2H2O(g);△H12H2(g)+O2(g)=2H2O(l);△H2 | ||||
| D、S(g)+O2(g)=SO2(g);△H1 S(s)+O2(g)=SO2(g);△H2 |
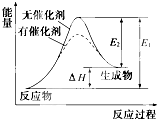 某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能).下列有关叙述正确的是( )| A、催化剂能改变该反应的焓变 |
| B、催化剂能降低该反应的活化能 |
| C、该反应为放热反应 |
| D、逆反应的活化能大于正反应的活化能 |
下列反应的离子方程式正确的是 ( )
| A、向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3↓+3H+ |
| B、用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| C、将氯气通入NaOH溶液中制取84消毒液:2Cl2+2OH-=ClO-+3Cl-+H2O |
| D、向Na2O2固体中滴加水:Na2O2+H2O=2Na++2OH-+O2↑ |
下列说法正确的是( )
| A、O2、O3互为同位素 |
| B、乙烷、乙烯互为同分异构体 |
| C、正丁烷和异丁烷互为同系物 |
| D、1H、2H、3H、H+、H2是氢元素形成的五种不同粒子 |