题目内容
20.实验室制得的乙烯气体中常含有少量的SO2,有人设计如下实验装置确认反应生成的气体中有乙烯和SO2.可供选择的试剂有:品红、NaOH溶液、溴水、浓硫酸.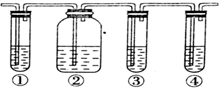
(1)①-④装置中所盛放的试剂(可重复)依次是品红、NaOH溶液、品红、溴水.
(2)确认有乙烯存在的现象是③中的品红不褪色,④中的溴水褪色.
(3)写出装置④中发生反应的化学方程式(用结构简式)CH2=CH2+Br2→CH2Br-CH2Br.
分析 确认反应生成的气体中有乙烯和SO2,二者均与溴水反应,由实验装置可知,①中Wie品红,品红褪色可说明含SO2,②中NaOH溶液除去SO2,③中品红检验SO2除尽,④中为溴水,溴水褪色可说明含乙烯,以此来解答.
解答 解:确认反应生成的气体中有乙烯和SO2,二者均与溴水反应,由实验装置可知,①中Wie品红,品红褪色可说明含SO2,②中NaOH溶液除去SO2,③中品红检验SO2除尽,④中为溴水,溴水褪色可说明含乙烯,
(1)由上述分析可知,①-④装置中所盛放的试剂(可重复)依次是品红、NaOH溶液、品红、溴水,
故答案为:品红、NaOH溶液、品红、溴水;
(2)确认有乙烯存在的现象是③中的品红不褪色,④中的溴水褪色,
故答案为:③中的品红不褪色,④中的溴水褪色;
(3)装置④中发生反应的化学方程式为CH2=CH2+Br2→CH2Br-CH2Br,
故答案为:CH2=CH2+Br2→CH2Br-CH2Br.
点评 本题考查性质实验方案的设计,为高频考点,把握实验装置的作用、物质的检验和发生的反应和现象为解答的关键,侧重分析与实验能力的考查,注重元素化合物与实验结合的训练,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.据报道,铀是一种放射性元素,23592U是核电站的主要燃料.下列关于23592U的说法正确的是( )
| A. | 质量数为235 | B. | 质子数是235 | ||
| C. | 中子数为92 | D. | 与23892U是同种原子 |
8. 如图所示的装置中,M为活动性顺序表中位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是( )
如图所示的装置中,M为活动性顺序表中位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是( )
 如图所示的装置中,M为活动性顺序表中位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是( )
如图所示的装置中,M为活动性顺序表中位于氢之前的金属,N为石墨棒,关于此装置的下列叙述中,不正确的是( )| A. | 导线中有电流通过,电流方向是由N到M | |
| B. | N上有气体放出 | |
| C. | M为正极,N为负极 | |
| D. | 是化学能转变为电能的装置 |
12.化学与生活、社会密切相关,下列说法正确的是( )
| A. | 铝表面有一层致密的氧化物薄膜,故铝制容器可用来腌制咸菜等 | |
| B. | 如果发生氯气泄漏,附近人员应迅速远离液氯泄漏地点,并顺风往低洼区域疏散 | |
| C. | “低碳生活”倡导生活中尽量减少耗能,从而减少CO2排放 | |
| D. | 向煤中加入适量CaSO4,可大大减少燃烧产物中SO2的量 |
9.下列说法中正确的是( )
| A. | 按系统命名法,化合物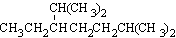 的名称为2,6-二甲基-5-乙基庚烷 的名称为2,6-二甲基-5-乙基庚烷 | |
| B. | 苯和油脂均不能使酸性KMnO4溶液褪色 | |
| C. | 有机物X的蒸气相对氢气的密度为51,X中氧元素的质量分数为31.7%,则能在碱性溶液中发生反应的X的同分异构体有(不考立体异构)13种 | |
| D. | 检验卤代烃中的卤素原子种类的方法是:加入NaOH溶液共热,再加AgNO3溶液,观察沉淀颜色 |
8.影响化学反应速率的因素很多,某课外兴趣小组用实验的方法进行探究.
实验一:甲同学利用Al、Fe、Mg和2mol/L的稀硫酸,设计实验方案研究影响反应速率的因素.研究的实验报告如下表:
(1)该同学的实验目的是探究反应物本身的性质对反应速率的影响;
要得出正确的实验结论,还需控制的实验条件是温度相同.
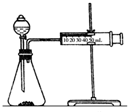
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图装置同温下进行定量实验,用大小形状相同的Fe分别和0.5mol/L及2mol/L的足量稀H2SO4反应,通过测定和比较同时间内产生氢气的体积可以说明浓度对化学反应速率的影响.
实验二:已知2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快.从影响化学反应速率的因素看,你猜想还可能是Mn2+的催化作用的影响.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入B.
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水.
实验一:甲同学利用Al、Fe、Mg和2mol/L的稀硫酸,设计实验方案研究影响反应速率的因素.研究的实验报告如下表:
| 实验步骤 | 现象 | 结论 |
| ①分别取等体积的2mol/L的硫酸于试管中;②分别投入大小、形状相同的Al、Fe、Mg | 反应快慢:Mg>Al>Fe | 反应物的性质越活泼,反应速率越快 |
要得出正确的实验结论,还需控制的实验条件是温度相同.
(2)乙同学为了更精确地研究浓度对反应速率的影响,利用如图装置同温下进行定量实验,用大小形状相同的Fe分别和0.5mol/L及2mol/L的足量稀H2SO4反应,通过测定和比较同时间内产生氢气的体积可以说明浓度对化学反应速率的影响.

实验二:已知2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+8H2O+10CO2↑,在开始一段时间内,反应速率较慢,溶液褪色不明显;但不久突然褪色,反应速率明显加快.
(1)针对上述现象,某同学认为该反应放热,导致溶液温度上升,反应速率加快.从影响化学反应速率的因素看,你猜想还可能是Mn2+的催化作用的影响.
(2)若用实验证明你的猜想,除酸性高锰酸钾溶液、草酸溶液外,可以在反应一开始时加入B.
A.硫酸钾 B.硫酸锰 C.氯化锰 D.水.
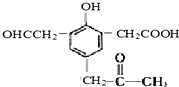 ,试回答:
,试回答: