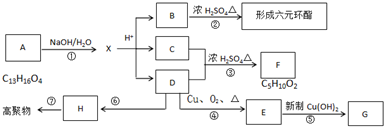
题目内容
化学实验是研究物质性质的基础.
(1)下列有关实验操作或测量数据合理的是 (填序号).
a.用铁坩埚加热CuSO4?5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8mL的Na2CO3溶液
(2)某废水样品中含有一定量的Na+、CO32-、SO32-,某研究小组欲测定其中SO32-的浓度.
实验方案:
ⅰ.用烧杯盛取废水适量,加少量活性炭,除去废水中的杂质;过滤,取滤液;
ⅱ.精确量取20.00mL过滤后废水试样,选择使用紫色的0.1mol/L KMnO4(H2SO4酸化)溶液进行滴定;
ⅲ.记录数据,计算.
①下列滴定方式中,最合理的是(夹持部已分略去) (填字母序号).
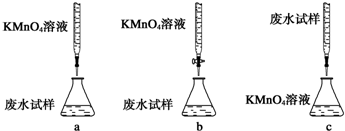
②滴定过程中,有关反应的离子方程式是 .
(3)某同学制备Fe(OH)3胶体:用洁净的烧杯取适量蒸馏水加热至沸腾,向烧杯中滴加1mol/L的FeCl3溶液,并不断用玻璃棒搅拌,结果溶液变浑浊.该同学制备胶体失败的原因是 ,你认为成功制得Fe(OH)3胶体的特征现象是 .
(4)用如图装置进行CO2性质的有关实验.
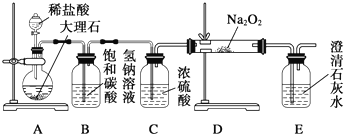
①试剂瓶B中盛有饱和NaHCO3溶液,其目的是: .
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系: .
(1)下列有关实验操作或测量数据合理的是
a.用铁坩埚加热CuSO4?5H2O晶体测定结晶水质量分数
b.用干燥的pH试纸测定浓硫酸的pH
c.用规格为20mL的量筒,量取16.8mL的Na2CO3溶液
(2)某废水样品中含有一定量的Na+、CO32-、SO32-,某研究小组欲测定其中SO32-的浓度.
实验方案:
ⅰ.用烧杯盛取废水适量,加少量活性炭,除去废水中的杂质;过滤,取滤液;
ⅱ.精确量取20.00mL过滤后废水试样,选择使用紫色的0.1mol/L KMnO4(H2SO4酸化)溶液进行滴定;
ⅲ.记录数据,计算.
①下列滴定方式中,最合理的是(夹持部已分略去)

②滴定过程中,有关反应的离子方程式是
(3)某同学制备Fe(OH)3胶体:用洁净的烧杯取适量蒸馏水加热至沸腾,向烧杯中滴加1mol/L的FeCl3溶液,并不断用玻璃棒搅拌,结果溶液变浑浊.该同学制备胶体失败的原因是
(4)用如图装置进行CO2性质的有关实验.

①试剂瓶B中盛有饱和NaHCO3溶液,其目的是:
②反应过程中,E中澄清石灰水变浑浊,E中的混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系:
考点:探究物质的组成或测量物质的含量,性质实验方案的设计
专题:实验设计题
分析:(1)a.铁会和CuSO4发生置换反应;
b.浓硫酸有脱水性,可以使pH试纸脱水碳化;
C.量筒精确到0.1;
(2)①酸性高锰酸钾具有强氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管内,废水样品中含有一定量的Na+、CO32-、SO32-,呈碱性,溶液由无色变为有色,现象明显;
②高锰酸钾能将亚硫酸根氧化为硫酸根;
(3)搅拌能使胶体聚沉;将饱和的FeCl3溶液滴入沸水中,加热直到得到红褐色溶液;
(4)实验流程为A装置制取二氧化碳,B、C装置净化二氧化碳,D装置验证二氧化碳性质,E装置检验二氧化碳.
①根据实验目的来分析仪器B加入饱和的NaHCO3溶液的目的;
②根据沉淀溶解平衡的书写方法写出,注意固体稀溶液的标注方法.
b.浓硫酸有脱水性,可以使pH试纸脱水碳化;
C.量筒精确到0.1;
(2)①酸性高锰酸钾具有强氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管内,废水样品中含有一定量的Na+、CO32-、SO32-,呈碱性,溶液由无色变为有色,现象明显;
②高锰酸钾能将亚硫酸根氧化为硫酸根;
(3)搅拌能使胶体聚沉;将饱和的FeCl3溶液滴入沸水中,加热直到得到红褐色溶液;
(4)实验流程为A装置制取二氧化碳,B、C装置净化二氧化碳,D装置验证二氧化碳性质,E装置检验二氧化碳.
①根据实验目的来分析仪器B加入饱和的NaHCO3溶液的目的;
②根据沉淀溶解平衡的书写方法写出,注意固体稀溶液的标注方法.
解答:
解:(1)a.用铁坩埚加热CuSO4?5H2O,铁会和CuSO4发生置换反应,造成误差,故a错误;
b.不能用干燥的pH试纸测定浓硫酸的pH,浓硫酸有脱水性,可以使pH试纸脱水碳化,不能与标准比色卡比较,故b错误;
C.量筒精确到0.1,可量取16.8mL的Na2CO3溶液,故c正确;
故答案为:c;
(2)①酸性高锰酸钾具有强氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管内,溶液由无色变为有色,现象明显,应用高锰酸钾滴定废水,
故答案为:b;
②高锰酸钾能将亚硫酸根氧化为硫酸根:5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O,
故答案为:5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O;
(3)制备Fe(OH)3胶体时,将饱和的FeCl3溶液滴入沸水中,加热直到得到红褐色溶液,不能搅拌,
故答案为:搅拌导致胶体聚沉;液体呈透明的红褐色;
(4)①根据实验目的来分析,反应生成的二氧化碳中含有氯化氢和水蒸气杂质气体,仪器B加入饱和的NaHCO3溶液的目的除去二氧化碳中的HCl气体;
故答案为:除去二氧化碳中的HCl气体;
②将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,得到碳酸钙沉淀,碳酸钙的溶解平衡为CaCO3(s)?Ca2+(aq)+CO32-(aq),
故答案为:CaCO3(s)?Ca2+(aq)+CO32-(aq).
b.不能用干燥的pH试纸测定浓硫酸的pH,浓硫酸有脱水性,可以使pH试纸脱水碳化,不能与标准比色卡比较,故b错误;
C.量筒精确到0.1,可量取16.8mL的Na2CO3溶液,故c正确;
故答案为:c;
(2)①酸性高锰酸钾具有强氧化性,可以腐蚀橡皮管,应盛放在酸式滴定管内,溶液由无色变为有色,现象明显,应用高锰酸钾滴定废水,
故答案为:b;
②高锰酸钾能将亚硫酸根氧化为硫酸根:5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O,
故答案为:5SO32-+2MnO4-+6H+=5SO42-+2Mn2++3H2O;
(3)制备Fe(OH)3胶体时,将饱和的FeCl3溶液滴入沸水中,加热直到得到红褐色溶液,不能搅拌,
故答案为:搅拌导致胶体聚沉;液体呈透明的红褐色;
(4)①根据实验目的来分析,反应生成的二氧化碳中含有氯化氢和水蒸气杂质气体,仪器B加入饱和的NaHCO3溶液的目的除去二氧化碳中的HCl气体;
故答案为:除去二氧化碳中的HCl气体;
②将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,得到碳酸钙沉淀,碳酸钙的溶解平衡为CaCO3(s)?Ca2+(aq)+CO32-(aq),
故答案为:CaCO3(s)?Ca2+(aq)+CO32-(aq).
点评:本题考查化学实验方案的评价及性质实验方案的设计,侧重于学生的分析能力和实验能力的考查,为高考常见题型,注意相关知识的学习与积累,难度不大.

练习册系列答案
相关题目
称取两份铝粉,第一份加入足量的NaOH溶液,第二份加入足量的盐酸溶液,如果要得到相同体积 (同温同压)的氢气,则两份铝粉的质量比是( )
| A、1:1 | B、1:2 |
| C、3:4 | D、2:5 |
石英光导纤维的主要成分是( )
| A、Si |
| B、SiC |
| C、SiO2 |
| D、Na2SiO3 |
设NA为阿伏伽德罗常数的值,下列叙述错误的是( )
| A、通常情况下,87g丙酮分子中含有的π键键数为1.5NA |
| B、标准状况下,11.2 L三氯甲烷分子中含有的σ键键数为2NA |
| C、2.5 mol乙醛与足量的氢气完全加成,断裂的π键键数为2.5NA |
| D、15 g 氨基乙酸通过成肽反应全部生成二肽时,生成的肽键键数为0.1NA |
检验某溶液中是否含有SO42-时,为防止Ag+、CO32-、SO32-等离子的干扰,下列实验方案比较严密的是( )
| A、先加稀HCl将溶液酸化,再滴加BaCl2溶液,看是否生成白色沉淀 |
| B、先加稀HNO3将溶液酸化,再滴加BaCl2溶液,看是否生成白色沉淀 |
| C、向溶液中滴加稀盐酸酸化的BaCl2溶液,看是否生成白色沉淀 |
| D、向溶液中滴加稀硝酸酸化的BaCl2溶液,看是否生成白色沉淀 |
食品卫生与身体健康密切相关,下列做法中对人体健康不会造成危害的是( )
| A、食品中添加苏丹红 |
| B、用小苏打做发酵粉 |
| C、福尔马林(35%-40%甲醛水溶液)浸泡海产品 |
| D、用硫磺薰制白木耳用 |