题目内容
 向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m克与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法正确的是( )
向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,产生沉淀的质量m克与加入Ba(OH)2的物质的量n之间的关系如图所示,下列说法正确的是( )| A、a→b时的沉淀成分为BaSO4与Mg(OH)2 |
| B、原混合溶液中:n(HCl)=2mol |
| C、c点时的溶液中c(Cl-)>c(OH-)>c(Ba2+) |
| D、b→c时发生的离子反应为H++OH-=H2O |
考点:有关混合物反应的计算
专题:
分析:向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,开始阶段发生的反应为:Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,对应图象为a-b段;
图象b-c段中沉淀不变,消耗了1mol氢氧化钡,说明发生反应:H++OH-=H2O,则此时消耗氢离子为2mol;
c-d段加入1mol氢氧化钡,沉淀物质的量增加,发生反应为:Mg2++2OH-=Mg(OH)2↓,说明原溶液中含有镁离子1mol;
d-e段沉淀的量不变,说明此时镁离子完全沉淀,据此进行解答.
图象b-c段中沉淀不变,消耗了1mol氢氧化钡,说明发生反应:H++OH-=H2O,则此时消耗氢离子为2mol;
c-d段加入1mol氢氧化钡,沉淀物质的量增加,发生反应为:Mg2++2OH-=Mg(OH)2↓,说明原溶液中含有镁离子1mol;
d-e段沉淀的量不变,说明此时镁离子完全沉淀,据此进行解答.
解答:
解:向含有一定量盐酸和少量MgSO4的混合溶液中逐滴加入Ba(OH)2溶液,开始阶段发生的反应为:Ba2++SO42-+2H++2OH-=BaSO4↓+2H2O,对应图象为a-b段;图象b-c段中沉淀不变,消耗了1mol氢氧化钡,说明发生反应:H++OH-=H2O,此过程中消耗2mol氢离子;c-d段加入1mol氢氧化钡,沉淀物质的量增加,发生反应为:Mg2++2OH-=Mg(OH)2↓,说明原溶液中含有镁离子1mol;d-e段沉淀的量不变,说明此时镁离子完全沉淀,
A.根据分析可知,a→b时的沉淀成分为BaSO4,故A错误;
B.a-b段、b-c段总共消耗2mol氢氧化钡,说明原混合液中含有4molHCl,故B错误;
C.c点时为氯化镁、氯化钡的混合液,氢氧根离子浓度非常小,则离子浓度大小为:c(Cl-)>c(Ba2+)>c(OH-),故C错误;
D.根据分析可知,b→c时发生的离子反应为:H++OH-=H2O,故D正确;
故选D.
A.根据分析可知,a→b时的沉淀成分为BaSO4,故A错误;
B.a-b段、b-c段总共消耗2mol氢氧化钡,说明原混合液中含有4molHCl,故B错误;
C.c点时为氯化镁、氯化钡的混合液,氢氧根离子浓度非常小,则离子浓度大小为:c(Cl-)>c(Ba2+)>c(OH-),故C错误;
D.根据分析可知,b→c时发生的离子反应为:H++OH-=H2O,故D正确;
故选D.
点评:本题考查了混合物反应的计算,侧重考查离子反应的计算,题目难度中等,明确发生反应的先后顺序为解答关键,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
下列说法中正确的是( )
| A、同一原子中,2p,3p,4p能级的轨道依次增多 |
| B、3p2表示3p能级有两个轨道 |
| C、同一原子中,1s,2s,3s电子的能量逐渐减小 |
| D、处于最低能量的原子叫做基态原子 |
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍,下列说法正确的是( )
| A、X的氢化物溶于水生成弱酸 |
| B、Z的氢化物的水溶液在空气中存放不易变质 |
| C、Y与X可生成Y3X2型化合物 |
| D、Z的单质在氧气中燃烧可以生成两种酸性氧化物 |
将一定质量的Mg,Zn,Al混合物与足量稀H2SO4反应,生成H2 2.8L(标准状况),原混合物的质量可能是( )
| A、2g | B、4g |
| C、10g | D、12g |
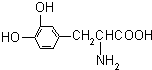 L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:
L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴酸碱性的叙述正确的是( )
| A、既没有酸性,又没有碱性 |
| B、既具有酸性,又具有碱性 |
| C、只有酸性,没有碱性 |
| D、只有碱性,没有酸性 |
 合成
合成 (部分试剂和反应条件已去).
(部分试剂和反应条件已去).
 ,写出在同条件CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式:
,写出在同条件CH2=CH-CH=CH2与等物质的量Br2发生加成反应的化学方程式: 的化学方程式(有机物写结构简式,注明条件).
的化学方程式(有机物写结构简式,注明条件). B.
B. C.
C.

 ,请填写下列空格:
,请填写下列空格: 物质中铁含量的测定方法是多种多样的.
物质中铁含量的测定方法是多种多样的. )结合显橙红色,再用比色法测定.其中涉及以下反应:4FeCl3+2NH2OH?HCl═4FeCl2+N2O↑+6HCI+H2O
)结合显橙红色,再用比色法测定.其中涉及以下反应:4FeCl3+2NH2OH?HCl═4FeCl2+N2O↑+6HCI+H2O 和邻啡罗啉都是含氮的有机物,l mol吡啶中含有Q键的物质的量为
和邻啡罗啉都是含氮的有机物,l mol吡啶中含有Q键的物质的量为