题目内容
测定铜合金中铜的含量,可以用稀硝酸来溶解样品,也可以用双氧水和稀盐酸溶解样品,其反应的化学方程式为:Cu+H2O2+2HCl===CuCl2+2H2O。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
(1)写出铜与稀硝酸反应的离子方程式并标出电子转移的方向和数目________________________________________________________________________。
(2)在铜与双氧水、盐酸的反应中氧化剂是________,若有2 mol的H2O2参加反应,则电子转移的物质的量是______________。
(3)用双氧水和稀盐酸溶解样品与用稀硝酸溶解样品相比较,哪种更好?为什么?
________________________________________________________________________。

(2)双氧水 4 mol
(3)双氧水更好,因为双氧水在酸性条件下氧化单质铜后的产物中没有污染空气的有害气体
【解析】
试题分析:化学反应中常用的氧化剂如高锰酸钾、浓硫酸、浓硝酸等,都会带来大量有害副产物,而以过氧化氢为氧化剂的还原产物是水,因此,过氧化氢有“清洁先生”的称谓。
考点:考查氧化还原反应方程式的表示、判断以及实验评价
点评:该题是中等难度的试题,也是高考中的常见题型。试题综合性强,主要是考查学生对氧化还原反应含义及有关判断的熟悉了解程度,侧重对学生实验能力的培养和训练,有利于培养学生的逻辑推理能力和规范、严谨的实验设计和操作能力,有利于提升学生的学科素养,调动学生的学习积极性。

| |||||||||||
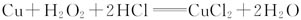 。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。 。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。
。假设样品中其他成分不与稀硝酸、双氧水和盐酸反应。