题目内容
1.有镁、铝和铁的混合物6.7g,与足量烧碱溶液共热后,在标准状况下产生3.36L氢气,将剩余溶液过滤后,残渣与足量稀硫酸反应,在标准状况下又产生2.24L氢气.求混合物中各物质的物质的量分数.分析 有镁、铝和铁的混合物6.7g,与足量烧碱溶液共热后,只有Al与氢氧化钠反应生成氢气,根据生成的氢气计算混合物中Al的物质的量;将剩余溶液过滤后,残渣为Mg、Fe,根据二者质量、电子转移守恒列方程计算Mg、Fe物质的量.
解答 解:有镁、铝和铁的混合物6.7g,与足量烧碱溶液共热后,只有Al与氢氧化钠反应生成氢气,生成氢气为$\frac{3.36L}{22.4L/mol}$=0.15mol,则Al的物质的量为$\frac{0.15mol×2}{3}$=0.1mol,
将剩余溶液过滤后,残渣为Mg、Fe,Al的质量为0.1mol×27g/mol=2.7g,则混合物中Mg、Fe总质量为6.7g-2.7g=4g,与硫酸反应生成氢气为$\frac{2.24L}{22.4L/mol}$=0.1mol,设Mg、Fe的物质的量分别为xmol、ymol,根据二者质量、电子转移守恒,则:$\left\{\begin{array}{l}{2x+2y=0.1×2}\\{24x+56y=4}\end{array}\right.$,解得x=y=0.05,
故混合物中Al的物质的量分数为$\frac{0.1mol}{(0.1+0.05+0.05)mol}$×100%=50%,
Mg、Fe的物质的量分数为$\frac{0.05mol}{(0.1+0.05+0.05)mol}$×100%=25%,
答:混合物中Al的物质的量分数为50%,Mg、Fe的物质的量分数均为25%.
点评 本题考查混合物有关计算,难度不大,注意利用电子转移守恒解答,避免方程式的繁琐.

练习册系列答案
相关题目
11.用含有A1203.SiO2和少量FeO•xFe2O3的铝灰制备A12(SO4)3•18H2O.工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩.结晶.分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:
生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol•L-1
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
Ⅰ.向铝灰中加入过量稀H2SO4,过滤:
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ.浓缩.结晶.分离,得到产品.
(1)H2S04溶解A1203的离子方程式是Al2O3+6H+=2Al3++3H2O
(2)KMnO4-氧化Fe2+的离子方程式补充完整:
1MnO4-+5Fe2++8H+=1Mn2++5Fe3++4H2O
(3)已知:
生成氢氧化物沉淀的pH
| Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 3.4 | 6.3 | 1.5 |
| 完全沉淀时 | 4.7 | 8.3 | 2.8 |
根据表中数据解释步骤Ⅱ的目的:pH约为3时,Fe2+和Al3+不能形成沉淀,将Fe2+氧化为Fe3+,可使铁完全沉淀
(4)己知:一定条件下,MnO4-可与Mn2+反应生成MnO2,
①向Ⅲ的沉淀中加入浓HCI并加热,能说明沉淀中存在MnO2的现象是生成黄绿色气体.
②Ⅳ中加入MnS04的目的是除去过量的MnO4-.
12.向含有1molFeCl2的溶液中通入0.2molCl2,再加入含0.1molX2O72-的酸性溶液,使溶液中Fe2+恰好全部被氧化为Fe3+,并使X2O72-还原为X3+,则n值为( )
| A. | 2 | B. | 3 | C. | 4 | D. | 6 |
16.常温下,0.1mol•L-1某一元酸(HA)溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-10,下列叙述正确的是( )
| A. | 溶液中水电离出的c(H+)=10-10 mol•L-1 | |
| B. | 溶液中c(H+)+c(A-)=0.1 mol•L-1 | |
| C. | 与0.05 mol•L-1 NaOH溶液等体积混合,水的电离平衡向正向移动 | |
| D. | 上述溶液中加入一定量NaA晶体或加水稀释,溶液的c(OH-)均增大 |
6.反应A(g)+3B(g)?2C(g)△H<0,达平衡后,将反应体系的温度升高,下列叙述中正确的是( )
| A. | 逆反应速率增大更大,平衡向逆反应方向移动 | |
| B. | 正反应速率增大更大,平衡向正反应方向移动 | |
| C. | 正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 | |
| D. | 正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
13.下列反应中,HCl只作还原剂的是( )
| A. | Zn+2HCl═ZnCl2+H2↑ | B. | O2+4HCl═2Cl2+2H2O | ||
| C. | MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O | D. | 2HCl═Cl2+H2 |
10.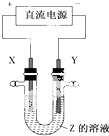 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
 利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )
利用如图所示装置,当X、Y选用不同材料时,可将电解原理广泛应用于工业生产.下列说法中正确的是( )| A. | 外加电流的阴极保护法中,Y是待保护金属 | |
| B. | 铜的精炼中,X是纯铜,Y是粗铜,Z是CuSO4 | |
| C. | 电镀工业中,X是待镀金属,Y是镀层金属 | |
| D. | 氯碱工业中,X、Y均为石墨,X附近能得到氢氧化钠 |
11.物质A~E均含同种元素,都是中学化学中常见的物质,它们可发生如图所表示的反应.已知A是一种淡黄色的固体,B是银白色金属单质.
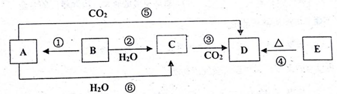
(1)反应⑤可用于潜水艇中制取氧气,相关的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,氧化剂是Na2O2,还原剂是Na2O2;
(2)根据反应②相关的现象,从表格下方找出相应性质序号填在表格中,并在对应的位置写上该反应的化学方程式.
与反应现象相应的性质:①反应后生成了酸性物质;②反应后生成了碱性物质;③单质B的熔点低;④单质B的密度比水的小;⑤生成了气体;⑥单质B的密度比水的密度大.
(3)D和E分别与等浓度的盐酸反应,相同条件下生成等体积的气体,则以下说法正确的是:①③(填序号)①消耗D的质量较多;②消耗E的质量较多;③D消耗盐酸的体积更大 ④E消耗盐酸的体积更大.

(1)反应⑤可用于潜水艇中制取氧气,相关的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,氧化剂是Na2O2,还原剂是Na2O2;
(2)根据反应②相关的现象,从表格下方找出相应性质序号填在表格中,并在对应的位置写上该反应的化学方程式.
| 现象 | 单质B的相关性质(填序号) | 相关的化学方程式 | |
| Ⅰ | 单质B浮在水面上 | ||
| Ⅱ | 熔成一个小球 | ||
| Ⅲ | 四处游动,发出嘶嘶的声音 | ||
| Ⅳ | 滴入酚酞试剂,溶液变红 |
(3)D和E分别与等浓度的盐酸反应,相同条件下生成等体积的气体,则以下说法正确的是:①③(填序号)①消耗D的质量较多;②消耗E的质量较多;③D消耗盐酸的体积更大 ④E消耗盐酸的体积更大.
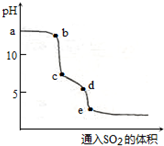 PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx.
PM2.5污染与直接排放化石燃烧产生的烟气有关,化石燃料燃烧同时放出大量的SO2和NOx.