题目内容
X元素的气态单质X2 10mL与Y元素的气态单质Y2 20mL均完全反应后生成气态物Z 20mL(气体体积均在相同条件下测得).气态物Z的分子式为( )
| A、XY |
| B、X2Y |
| C、XY2 |
| D、XY3 |
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:相同条件下,气体摩尔体积相等,同一反应的各物质体积之比等于其计量数之比,再结合原子守恒判断Z的分子式.
解答:
解:相同条件下,气体摩尔体积相等,同一反应的各物质体积之比等于其计量数之比,所以X2、Y2、Z的计量数之比=10mL:20mL:20mL=1:2:2,该反应方程式为X2+2Y2=2Z,根据原子守恒知,Z的化学式为XY2,故选C.
点评:本题考查阿伏伽德罗定律及推论,明确相同条件下气体体积与化学计量数的关系是解本题关键,并结合质量守恒定律判断即可,题目难度不大,注意气体摩尔体积的适用范围及适用条件.

练习册系列答案
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案
相关题目
不能用排水收集法收集的气体是( )
| A、氨气 | B、氧气 |
| C、二氧化硫 | D、一氧化氮 |
短周期元素W、X、Y、Z的原子序数依次增大,W与Y,X与Z分别位于同一主族,W与X可形成两种常见气体WX2和WX,Y原子的内层电子总数是其最外层电子数的2.5倍,下列叙述中不正确的是( )
| A、WX2分子中所有原子最外层都已满足8电子结构 |
| B、WX2、ZX2的化学键类型相同 |
| C、原子半径大小顺序为:X<W<Y<Z |
| D、乙醇、乙酸、葡萄糖、油脂中均含W、X两种元素 |
对于醋酸溶液的下列说法中,不正确的是( )
| A、醋酸溶液中离子浓度的关系满足:c(H+)═c(OH-)+c(CH3COO-) |
| B、醋酸溶液中加入少量醋酸钠晶体,醋酸电离程度减小 |
| C、0.1mol/L的醋酸溶液中加水稀释,溶液中c(OH-)减小 |
| D、常温下,pH=3的醋酸溶液与pH=11的烧碱溶液等体积混合后,溶液中c(H+)<c(OH-) |
25℃时,下列说法中,不正确的是( )
| A、将体积均为100mL、浓度均为0.1mol/L的Ba(OH)2溶液与Na2SO4溶液混合,若混合后溶液的体积为100mL,则所得溶液的pH=13 |
| B、将等体积等浓度的醋酸与CH3COONa溶液混合,所得溶液中:c(Na+)+c(H+)═c(CH3COO-)+c(OH-) |
| C、将等体积等浓度的Na2CO3溶液与NaHCO3溶液混合,所得溶液中:2c(Na+)═c(CO32-)+c(HCO3-)+c(H2CO3) |
| D、将等体积等浓度的Na2CO3溶液与NaOH溶液混合,所得溶液中:c(Na+)>c(OH-)>c(CO32-)>c(H+) |
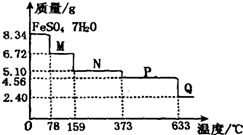 取8.34g FeS04?7H20样品加热,其受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则下列叙述中不正确的是( )
取8.34g FeS04?7H20样品加热,其受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,则下列叙述中不正确的是( )| A、温度为78℃时固体物质M的化学式为FeSO4?4H2O | ||||
| B、温度为l59℃时固体物质N的化学式为FeSO4?H2O | ||||
C、在隔绝空气条件下,N得到P的化学方程式为:FeSO4
| ||||
| D、固体P隔绝空气加热至650℃,得到一种固体物质Q,同时有三种无色气体生成,Q的化学式为Fe2O3 |
下列实验操作或装置符合实验要求的是( )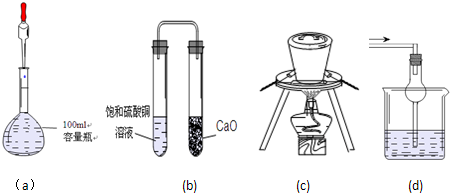

| A、(a) 可用于定容并量取15.00 mL NaOH溶液 |
| B、(b)装置放置一段时间后,饱和CuSO4溶液中出现蓝色晶体 |
| C、(c)可用于高温煅烧石灰石 |
| D、(d)可用于易溶于水的尾气吸收 |
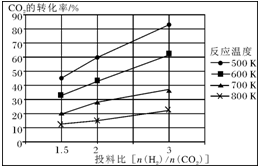 燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.
燃煤废气中的氮氧化物(NOx)、二氧化碳等气体,常用下列方法处理,以实现节能减排、废物利用等.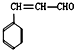 和化合物Ⅱ
和化合物Ⅱ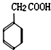 在一定条件下发生反应能生成化合物Ⅲ
在一定条件下发生反应能生成化合物Ⅲ ,请回答以下问题.
,请回答以下问题.