题目内容
13.含4g氢氧化钠的溶液分别与盐酸、硫酸、磷酸反应生成正盐各需酸多少摩尔?分析 n(NaOH)=$\frac{4g}{40g/mol}$=0.1mol,结合HCl+NaOH=NaCl+H2O、H2SO4+2NaOH=Na2SO4+2H2O、H3PO4+3NaOH=Na3PO4+3H2O计算.
解答 解:n(NaOH)=$\frac{4g}{40g/mol}$=0.1mol,
由HCl+NaOH=NaCl+H2O可知,需要盐酸为0.1mol;
由H2SO4+2NaOH=Na2SO4+2H2O可知,需要硫酸为0.1mol×$\frac{1}{2}$=0.05mol;
由H3PO4+3NaOH=Na3PO4+3H2O可知,需要磷酸为0.1mol×$\frac{1}{3}$=0.033mol,
答:含4g氢氧化钠的溶液分别与盐酸、硫酸、磷酸反应生成正盐各需酸为0.1mol、0.05mol、0.033mol.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应、物质的量关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
4.Na2CO3的摩尔质量为106g•mol-1.将5.3gNa2CO3固体完全溶于稀盐酸后,再用蒸馏水稀释成100mL溶液.该溶液中Na+的物质的量浓度为( )
| A. | 5.0mol•L-1 | B. | 0.10mol•L-1 | C. | 1.0mol•L-1 | D. | 0.50mol•L-1 |
1.聚碳酸酯 的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼睛镜片、光盘、唱片等.原来合成聚碳酸酯的一种原料是用有毒的光气(又称碳酰氯COCl2),现在改用绿色化学原料碳酸二甲酯
的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼睛镜片、光盘、唱片等.原来合成聚碳酸酯的一种原料是用有毒的光气(又称碳酰氯COCl2),现在改用绿色化学原料碳酸二甲酯  与哪类物质缩合聚合而成( )
与哪类物质缩合聚合而成( )
 的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼睛镜片、光盘、唱片等.原来合成聚碳酸酯的一种原料是用有毒的光气(又称碳酰氯COCl2),现在改用绿色化学原料碳酸二甲酯
的透光率良好,可制作车、船、飞机的挡风玻璃,以及眼睛镜片、光盘、唱片等.原来合成聚碳酸酯的一种原料是用有毒的光气(又称碳酰氯COCl2),现在改用绿色化学原料碳酸二甲酯  与哪类物质缩合聚合而成( )
与哪类物质缩合聚合而成( )| A. | 二卤代物 | B. | 二酚类 | C. | 二醛类 | D. | 二烯类 |
8.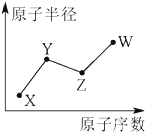 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y是形成化合物种类最多的元素,Z与X可形成两种常温下液态的化合物,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y是形成化合物种类最多的元素,Z与X可形成两种常温下液态的化合物,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
 X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y是形成化合物种类最多的元素,Z与X可形成两种常温下液态的化合物,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )
X、Y、Z、W是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示.已知Y是形成化合物种类最多的元素,Z与X可形成两种常温下液态的化合物,W原子的最外层电子数与Ne原子的最外层电子数相差1.下列说法正确的是( )| A. | Y、Z、W三种元素只可能形成3种化合物 | |
| B. | X、Y、Z三种元素可形成的化合物超过8种 | |
| C. | Y、W的含氧酸的酸性:Y<W | |
| D. | 1molX、Y两种元素形成的化合物充分燃烧,消耗氧气就是2mol |
16.柠檬烯是一种食用香料,其结构简式如图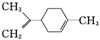 所示.有关柠檬烯的分析正确的是( )
所示.有关柠檬烯的分析正确的是( )
 所示.有关柠檬烯的分析正确的是( )
所示.有关柠檬烯的分析正确的是( )| A. | 它的一氯代物有6种 | |
| B. | 一定条件下,它分别可以发生加成、取代、氧化等反应 | |
| C. | 它的分子中所有的碳原子可能在同一平面上 | |
| D. | 它和丁基苯(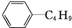 )互为同分异构体 )互为同分异构体 |
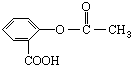 ,它可以接在一种高聚物载体上形成缓释长效药剂.其中的一种结构如下:
,它可以接在一种高聚物载体上形成缓释长效药剂.其中的一种结构如下: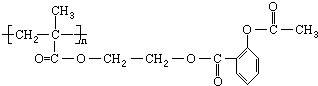
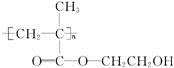 .
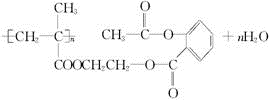
.
 .
.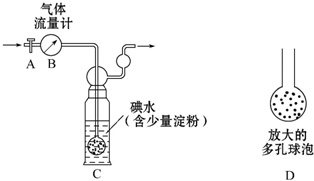 硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放.某化学研究性学习小组的同学欲采用以下方案测定硫酸工业尾气中SO2含量
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放.某化学研究性学习小组的同学欲采用以下方案测定硫酸工业尾气中SO2含量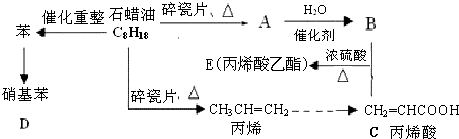
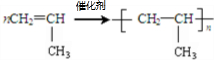 ;反应类型加聚反应.
;反应类型加聚反应.