题目内容
4.下列物质的熔沸点高低顺序正确的是( )| A. | 金刚石>晶体硅>碳化硅 | B. | KCl>NaCl>LiCl | ||
| C. | H2O>H2Se>H2S | D. | CCl4>CBr4>CI4 |
分析 一般来说,熔沸点为原子晶体>离子晶体>金属晶体>分子晶体,
A.原子晶体中,共价键越短,熔沸点越大;
B.离子晶体中,离子半径越短,熔沸点越大;
C.水中含氢键沸点最高,氢化物的相对分子质量越大,熔沸点越大;
D.分子晶体的相对分子质量越大,熔沸点越大.
解答 解:A.均为原子晶体,熔沸点为金刚石>碳化硅>晶体硅,故A错误;
B.均为离子晶体,熔沸点为KCl<NaCl<LiCl,故B错误;
C.均为分子晶体,水中含氢键,则熔沸点为H2O>H2Se>H2S,故C正确;
D.均为分子晶体,则熔沸点为CCl4<CBr4<CI4,故D错误;
故选C.
点评 本题考查晶体性质的比较,为高频考点,把握晶体类型、熔沸点比较方法为解答的关键,侧重分析与应用能力的考查,注意不同晶体熔沸点比较方法不同,题目难度不大.

练习册系列答案
 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案
相关题目
14.下列有关化学实验的叙述正确的是( )
| A. | 配制FeCl3溶液时,向溶液中加入少量Fe屑和稀盐酸 | |
| B. | 可以用热的碳酸钠溶液清洗装过油脂的试管 | |
| C. | 利用苯与溴水混合振荡静置后溴水褪色实验,证明苯分子含有碳碳双键 | |
| D. | 用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸 |
15.下列气体在标准状况下,质量相同时体积最大的是( )
| A. | 氯气 | B. | 氢气 | C. | 氧气 | D. | 氮气 |
19.下列关于碳和硅的叙述中,不正确的是( )
| A. | 高价态氧化物都能与氢氧化钠溶液反应 | |
| B. | 氧化物都能溶于水生成相应的酸 | |
| C. | 单质在加热时都能跟氧气反应 | |
| D. | 碳和硅的单质常温下化学性质都不活泼 |
16. 25℃时,将浓度均为0.1mol/L CH3COOH溶液和HX溶液分别与等浓度的NaHCO3溶液等体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,则下列说法正确的是( )
25℃时,将浓度均为0.1mol/L CH3COOH溶液和HX溶液分别与等浓度的NaHCO3溶液等体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,则下列说法正确的是( )
 25℃时,将浓度均为0.1mol/L CH3COOH溶液和HX溶液分别与等浓度的NaHCO3溶液等体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,则下列说法正确的是( )
25℃时,将浓度均为0.1mol/L CH3COOH溶液和HX溶液分别与等浓度的NaHCO3溶液等体积混合,实验测得产生的气体体积(V)随时间(t)变化的示意图如图所示,则下列说法正确的是( )| A. | 电离平衡常数:CH3COOH>HX>H2CO3 | |
| B. | 将pH=2的CH3COOH溶液和HX溶液稀释10倍后,水电离出的c (H+)较大的为HX溶液 | |
| C. | 往10ml 0.1mol/L的Na2CO3溶液中缓慢滴加10ml 0.1mol/L的HX,混合后的离子浓度大小关系:c (Na+)>c (HCO3-)>c (X-)>c (OH-)>c (H+) | |
| D. | 将浓度均为0.1mol/L的CH3COOH和HX的混合液用标准氢氧化钠溶液滴定,至中性时,CH3COOH被完全中和 |
13.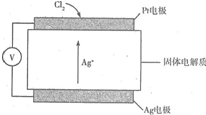 C12是一种重要的化工原料,氯气含量检测仪是检测Cl2是否泄漏不可或缺的安全性仪器,其工作原理如图所示,下列有关说法错误的是( )
C12是一种重要的化工原料,氯气含量检测仪是检测Cl2是否泄漏不可或缺的安全性仪器,其工作原理如图所示,下列有关说法错误的是( )
 C12是一种重要的化工原料,氯气含量检测仪是检测Cl2是否泄漏不可或缺的安全性仪器,其工作原理如图所示,下列有关说法错误的是( )
C12是一种重要的化工原料,氯气含量检测仪是检测Cl2是否泄漏不可或缺的安全性仪器,其工作原理如图所示,下列有关说法错误的是( )| A. | Pt电极为正极 | |
| B. | 电子从Ag电极经外电路流向Pt电极 | |
| C. | Ag电极的电极反应式是Cl2+2e-+2Ag+=2AgCl | |
| D. | 当电路中转移2 mol电子时,消耗1 mol Cl2 |
12.1869年,俄国化学家绘制出世界上第一张元素周期表.( )
| A. | 道尔顿 | B. | 拉瓦锡 | C. | 门捷列夫 | D. | 阿伏伽德罗 |
