题目内容
在氨水中存在平衡:NH3?H2O?NH4++OH-.若向其中分别加入少量下列物质(见下表),则该溶液中c(OH-)将如何变化?请将c(OH-)的变化结果填入下表(填“变大”、“变小”或“不变”).
| 加入的物质 | NaCl(s) | NaOH(s) | (NH4)2SO4(s) |
| c(OH-)的变化 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:氨水中存在平衡:NH3?H2O?NH4++OH-,向溶液中加入和铵根离子或氢氧根离子反应的物质促进一水合氨电离,加入含有铵根离子或氢氧根离子的物质抑制一水合氨电离,据此分析解答.
解答:
解:氨水中存在平衡:NH3?H2O?NH4++OH-,向溶液中加入和铵根离子或氢氧根离子反应的物质促进一水合氨电离,加入含有铵根离子或氢氧根离子的物质抑制一水合氨电离,
向氨水中加入氯化钠,溶液中一水合氨分子、铵根离子、氢氧根离子浓度都不变,则不影响平衡移动;
向溶液中加入氢氧化钠,氢氧化钠电离出氢氧根离子而使其溶液中氢氧根离子浓度增大,抑制一水合氨电离;
向溶液中加入硫酸铵,硫酸铵电离出铵根离子而抑制一水合氨电离,则溶液中氢氧根离子浓度减小,
故答案为:不变;变大;变小.
向氨水中加入氯化钠,溶液中一水合氨分子、铵根离子、氢氧根离子浓度都不变,则不影响平衡移动;
向溶液中加入氢氧化钠,氢氧化钠电离出氢氧根离子而使其溶液中氢氧根离子浓度增大,抑制一水合氨电离;
向溶液中加入硫酸铵,硫酸铵电离出铵根离子而抑制一水合氨电离,则溶液中氢氧根离子浓度减小,
故答案为:不变;变大;变小.
点评:本题考查了弱电解质的电离,根据加入物质是否影响弱电解质的电离平衡来确定溶液中离子浓度是否变化,题目难度不大.

练习册系列答案
相关题目
下列操作方法或实验装置正确的是( )
A、 探究NaHCO3的热稳定性 |
B、 NH3的收集 |
C、 向容量瓶中转移液体 |
D、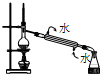 石油蒸馏 |
制备Fe(OH)3胶体的方法是,向沸水中加入饱和FeCl3,然后继续加热.检验是否已经得到胶体的最简单有效的方法是( )
| A、观察颜色和状态 |
| B、观察是否能产生丁达尔现象(效应) |
| C、加入足量的盐酸 |
| D、滴入氢氧化钠溶液 |
下列有机物互为同分异构体的是( )
| A、乙烯和聚乙烯 |
| B、淀粉和纤维素 |
| C、果糖和葡萄糖 |
| D、蛋白质和氨基酸 |
 往100mLNaOH溶液中通入CO2,充分反应后,在减压和较低温度下,小心将溶液蒸干,得白色固体M.通入标况下CO2的体积V(CO2)(单位:mL)与M的质量(w)(单位:g)的关系如图:
往100mLNaOH溶液中通入CO2,充分反应后,在减压和较低温度下,小心将溶液蒸干,得白色固体M.通入标况下CO2的体积V(CO2)(单位:mL)与M的质量(w)(单位:g)的关系如图: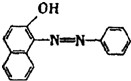 2005年4月10日,中央电视台发布“每周质量报告”,全国共有18个省市30家企业的88种食品样品中都检出了致癌物工业用染料“苏丹红I号”.苏丹红I号结构如图所示:
2005年4月10日,中央电视台发布“每周质量报告”,全国共有18个省市30家企业的88种食品样品中都检出了致癌物工业用染料“苏丹红I号”.苏丹红I号结构如图所示:
