题目内容
13.某烷烃的相对分子质量为72,其结构(同分异构体)有3种,1mol该烷烃完全燃烧需消耗氧气8 mol.分析 根据烷烃的通式CnH2n+2来计算,按碳链异构写出烷烃的同分异构体.根据烷烃燃烧通式为CnH2n+2+$\frac{3n+1}{2}$O2$\frac{点燃}{\;}$nCO2+(n+1)H2O确定消耗氧气.
解答 解:某烷烃的相对分子质量为72,烷烃的通式CnH2n+2,则14n+2=72,解得n=5,所以该烷烃的分子式为C5H12,
分子式为C5H12的同分异构体有主链有5个碳原子的:CH3CH2CH2CH2CH3,
主链有4个碳原子的: ,
,
主链有3个碳原子的: ;
;
1mol该C5H12完全燃烧需消耗氧气为1mol×$\frac{3×5+1}{2}$=8mol,
故答案为:3种;8.
点评 本题考查有机物分子式确定、同分异构体书写、烷烃的命名,比较基础,注意利用组成通式确定分子式,掌握烷烃同分异构体书写.

练习册系列答案
相关题目
13.下列物质中,不属于通常所说的三大合成材料的是( )
| A. | 塑料 | B. | 蛋白质 | C. | 合成纤维 | D. | 合成橡胶 |
14.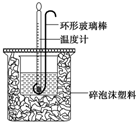 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
(1)碎泡沫塑料的作用是保温隔热,减少热量损失环形玻璃搅拌棒可不可以用铜丝搅拌棒代替,为什么不可以;铜的导热性好,易损失热量产生误差
(2)该实验测得的中和热数值为56.8 kJ•mol-1,(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算).
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值偏小(“偏大”、“偏小”或“不变”)
 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1 NaOH溶液和右图所示装置进行测定中和热的实验,得到表中的数据| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃[来源:Z,xx,k.Com] | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.3 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 20.5 | 20.6 | 24.9 |
(2)该实验测得的中和热数值为56.8 kJ•mol-1,(盐酸和NaOH溶液的密度按1g•cm-3计算,反应后混合溶液的比热容(c)按4.18J•(g•℃)-1计算).
(3)若将NaOH溶液改为相同体积、相同浓度的氨水,测得中和热的数值偏小(“偏大”、“偏小”或“不变”)
18.关于氢键,下列说法正确的是( )
| A. | 由于冰中的水分子间存在氢键,所以其密度大于液态水 | |
| B. | 可以用氢键解释接近沸点的水蒸气的相对分子质量测定值比用化学式(H2O)计算出来的相对分子质量大 | |
| C. | 分子间氢键和分子内氢键都会使熔沸点升高 | |
| D. | 每一个水分子内平均含有两个氢键 |
5.设NA为阿伏加德罗常数的值,下列说法错误的是( )
| A. | 1mol/L 的Na2CO3溶液中,含有的Na+离子数为2 NA | |
| B. | 0.5 mol H2SO4含有的原子数目为3.5NA | |
| C. | 32 g O2所含的分子数目为NA | |
| D. | 27g金属铝变成铝离子时失去的电子数为3NA |
2.某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行滴定操作:
选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是③.(填序号)除以上仪器外还缺的玻璃仪器有250mL容量瓶中、胶头滴管.
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
请完成下列问题:
(1)正确的操作步骤是(填写字母)C→A→B→D→E.
(2)滴定管读数应注意滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到0.01ml.
(3)操作中锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(4)操作D中液面应调整到调节到零刻度或零稍下的某一刻度,充满标准H2SO4溶液;
(5)滴定到终点时锥形瓶内溶液的pH约为4;终点时的颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响偏高(填“偏高”、“偏低”或“无影响”,其他操作均正确).
选用仪器如下:①量筒;②锥形瓶;③滴定管;④玻璃棒.上列仪器中在使用前需检查是否漏水的是③.(填序号)除以上仪器外还缺的玻璃仪器有250mL容量瓶中、胶头滴管.
操作步骤:
A.在250mL容量瓶中配制250mL烧碱溶液
B.用碱式滴定管量取25.00mL烧碱溶液于锥形瓶中并加几滴甲基橙指示剂
C.在天平上准确称取烧碱样品w g,在烧杯中加蒸馏水溶解
D.将物质的量浓度为m mol/L的标准H2SO4溶液装入酸式滴定管,调整液面,记下开始刻度V1 mL
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点刻度为V2 mL
附:酸碱指示剂变色范围
| 指示剂 | 变色范围 | 酸色 | 碱色 |
| 石蕊 | 5.0-8.0 | 红色 | 蓝色 |
| 酚酞 | 8.0-10.0 | 无色 | 红色 |
| 甲基橙 | 3.1-4.4 | 红色 | 黄色 |
(1)正确的操作步骤是(填写字母)C→A→B→D→E.
(2)滴定管读数应注意滴定管垂直,液面不再变化时才可读数,视线与溶液凹液面最低点相平,读数精确到0.01ml.
(3)操作中锥形瓶下垫一张白纸的作用是便于准确判断终点时颜色的变化情况.
(4)操作D中液面应调整到调节到零刻度或零稍下的某一刻度,充满标准H2SO4溶液;
(5)滴定到终点时锥形瓶内溶液的pH约为4;终点时的颜色变化是溶液由黄色变为橙色,且半分钟内不恢复为原来的颜色.
(6)若酸式滴定管没用标准H2SO4润洗,会对测定结果有何影响偏高(填“偏高”、“偏低”或“无影响”,其他操作均正确).
3.用铝制易拉罐手机满CO2后迅速加入过量浓NaOH溶液,立即把口封闭.发现易拉罐“咔咔”作响,并变瘪了,过一会儿后,易拉罐又会作响并鼓起来.下列说法正确的是( )
| A. | 导致易拉罐变瘪的离子反应是:CO2+OH-═HCO3- | |
| B. | 导致易拉罐又鼓起来的反应是:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑ | |
| C. | 若将CO2换为NH3,浓NaOH溶液换为水,易拉罐也会出现先瘪后鼓的现象 | |
| D. | 反应结束后,易拉罐内溶液中的溶质只有Na[Al(OH)4] |
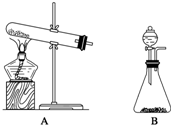 氨气是化学实验室常需制取的气体.实验室制取氨气通常有两种方法:
氨气是化学实验室常需制取的气体.实验室制取氨气通常有两种方法: