题目内容
化合物BrFx与水按物质的量之比3:5发生反应,其产物为溴酸、氢氟酸,单质溴和氧气.
(1)BrFx中,x= .
(2)该反应的化学方程式是 .
(3)此反应的氧化剂是 ,还原剂是 .
(1)BrFx中,x=
(2)该反应的化学方程式是
(3)此反应的氧化剂是
考点:氧化还原反应的计算
专题:
分析:BrFx与H2O按物质的量之比3:5反应的产物是HF、HBrO3、Br2、O2,则反应为3BrFx+5H2O=9HF+HBrO3+Br2+O2,由F原子守恒可知,x=3,Br元素的化合价由+3价降低为0,Br元素的化合价以由+3价升高为+5价,O元素的化合价由-2价升高为0,以此计算解答.
解答:
解:(1)BrFx与H2O按物质的量之比3:5反应的产物是HF、HBrO3、Br2、O2,则反应为3BrFx+5H2O=9HF+HBrO3+Br2+O2,由F原子守恒可知,x=3,
故答案为:3;
(2)由(1)可知反应为3BrF3+5H2O=9HF+HBrO3+Br2+O2↑,故答案为:3BrF3+5H2O=9HF+HBrO3+Br2+O2↑;
(3)Br元素的化合价由+3价降低为0,则氧化剂为BrF3,Br元素的化合价以由+3价升高为+5价,O元素的化合价由-2价升高为0,还原剂为BrF3、H2O,
故答案为:BrF3;BrF3、H2O.
故答案为:3;
(2)由(1)可知反应为3BrF3+5H2O=9HF+HBrO3+Br2+O2↑,故答案为:3BrF3+5H2O=9HF+HBrO3+Br2+O2↑;
(3)Br元素的化合价由+3价降低为0,则氧化剂为BrF3,Br元素的化合价以由+3价升高为+5价,O元素的化合价由-2价升高为0,还原剂为BrF3、H2O,
故答案为:BrF3;BrF3、H2O.
点评:本题考查氧化还原反应的计算,为高频考点,把握反应中元素的化合价变化及守恒计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
只需用一种试剂即可将酒精、苯酚溶液、苯、己烯四种无色液体区分开来,该试剂是( )
| A、FeCl3溶液 |
| B、溴水 |
| C、KMnO4溶液 |
| D、金属钠 |
向三份1mol/LNa2CO3溶液中分别加入少量NH4Cl、Na2S、FeCl3固体(忽略溶液体积变化),则CO32-浓度的变化依次为( )
| A、减小、增大、减小 |
| B、增大、减小、减小 |
| C、减小、增大、增大 |
| D、增大、减小、增大 |
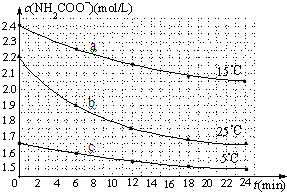 某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数.
某研究小组在实验室探究氨基甲酸铵(H2NCOONH4)水解反应速率的测定和分解反应平衡常数. 某化工厂用氯气与氢氧化钙生产漂白粉.该厂出厂产品说明书如图所示:
某化工厂用氯气与氢氧化钙生产漂白粉.该厂出厂产品说明书如图所示: