题目内容
16.设NA为阿佛加德罗常数,上述说法不正确的是( )①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤32gO2和O3混合气体中含有原子数为2NA.
| A. | ③④⑤ | B. | ①③④ | C. | ④ | D. | ③⑤ |
分析 ①求出标准状况下,11.2L混合气体的物质的量,然后根据氮气和氧气均为双原子分子来分析;
②同温同压下,体积相同的氢气和氩气的物质的量相同;
③求出氯化镁的物质的量,然后根据1mol氯化镁中含2mol氯离子来分析;
④根据标准状况下H2O为液态来分析;
⑤O2和O3均由氧原子构成来分析.
解答 解:①标准状况下,11.2L混合气体的物质的量为0.5mol,而氮气和氧气均为双原子分子,故0.5mol混合气体中含NA个原子,故①正确;
②同温同压下,体积相同的氢气和氩气的物质的量相同,根据分子个数N=nNA可知,分子个数也相同,故②正确;
③1L2mol/L氯化镁的物质的量n=CV=2mol/L×1L=2mol,而1mol氯化镁中含2mol氯离子,即2NA个,故③正确;
④标准状况下H2O为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故④错误;
⑤O2和O3均由氧原子构成,故32g混合物中含2mol氧原子,故含2NA个,故⑤正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
13.下列变化,是通过取代反应来实现的是( )
| A. | CH3CH2OH→CH3CHO | B. | CH2=CH2→CH3-CH2Br | ||
| C. | 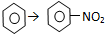 | D. | CH3CH2OH→CH3COOH |
7.现有八种短周期元素a~h的有关性质的数据如下
根据元素周期律,判断下列推断不正确的是( )
| 元素编号 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.093 |
| 最高化合价或最低化合价 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | -1 |
| A. | 元素a与元素c形成的化合物分子中的化学键是极性键 | |
| B. | b元素形成的氢化物分子间存在氢键 | |
| C. | e元素位于周期表中的第二周期ⅥA族 | |
| D. | 元素f的最高价氧化物的水化物能溶于元素h的最高价氧化物的水化物的水溶液中 |
11.如图是A、B两种物质的溶解度曲线,下列说法不正确的是( )


| A. | A物质的溶解度随温度升高而增大 | |
| B. | t2℃时,A物质的溶解度大于B物质的溶解度 | |
| C. | A的饱和溶液温度越高,溶质质量分数越大 | |
| D. | t1℃时,A、B两种物质饱和溶液的质量分数为25% |
8.下列化合物属于有机物的是( )
| A. | NaCN | B. | CaCO3 | C. | CO(NH2)2 | D. | NH4CNO |
5.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 选项 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 己烷(己烯) | 溴水 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | CH3CH2OH (CH3COOH) | CaO | 蒸馏 |
| D | CH3COOC2H5 (CH3COOH) | NaOH溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
6.下列化学用语正确的是( )
| A. | 基态碳原子的L层电子排布图: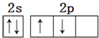 | |
| B. | 二氧化碳的电子式: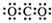 | |
| C. | 硫离子的结构示意图: | |
| D. | 质子数为35、中子数为45的溴原子:${\;}_{35}^{80}$Br |