题目内容
用NA表示阿伏德罗常数,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的分子数为 NA |
| B、常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA |
| C、通常状况下,NA 个CO2分子占有的体积为22.4L |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
考点:阿伏加德罗常数
专题:
分析:A.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
B.1.06g碳酸钠的物质的量为0.01mol,0.01mol碳酸钠中含有0.02mol钠离子;
C.通常状况下,NA个CO2分子的物质的量为1mol,不是标况下,不能使用标况下气体摩尔体积计算二氧化碳的体积;
D.缺少氯化镁溶液的体积,无法计算溶液中氯离子的数目.
B.1.06g碳酸钠的物质的量为0.01mol,0.01mol碳酸钠中含有0.02mol钠离子;
C.通常状况下,NA个CO2分子的物质的量为1mol,不是标况下,不能使用标况下气体摩尔体积计算二氧化碳的体积;
D.缺少氯化镁溶液的体积,无法计算溶液中氯离子的数目.
解答:
解:A.标况下水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故A错误;
B.1.06g碳酸钠的物质的量为:
=0.01mol,0.01mol碳酸钠中含有0.02mol钠离子,含有的Na+离子数为0.02 NA,故B正确;
C.NA个CO2分子的物质的量为1mol,不是标准状况下,不能使用标况下的气体摩尔体积计算1mol二氧化碳的体积,故C错误;
D.没有告诉氯化镁溶液的体积,无法计算溶液中含有氯离子的数目,故D错误;
故选B.
B.1.06g碳酸钠的物质的量为:
| 1.06g |
| 106g/mol |
C.NA个CO2分子的物质的量为1mol,不是标准状况下,不能使用标况下的气体摩尔体积计算1mol二氧化碳的体积,故C错误;
D.没有告诉氯化镁溶液的体积,无法计算溶液中含有氯离子的数目,故D错误;
故选B.
点评:本题考查阿伏加德罗常数的应用,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确标况下气体摩尔体积的使用条件:是否在标准状况下、标况下物质的状态是否为气体.

练习册系列答案
相关题目
一定温度下,对于反应N2+O2?2NO在密闭容器中进行,下列措施一定能加快反应速率的是( )
| A、使压强增大 |
| B、恒容,充入N2 |
| C、恒容,充入He气 |
| D、恒压,充入He气 |
下列关于钠的说法不正确的是( )
| A、金属钠和氧气反应,条件不同,产物不同 |
| B、钠长期置于空气中,表面不能形成致密氧化膜 |
| C、钠与水反应时,钠熔成小球在水面四处游动 |
| D、由于钠比较活泼,所以它能从溶液中置换出金属活动性顺序表中钠后面的金属 |
下列变化过程,属于放热过程的是( )
| A、酸碱中和反应 |
| B、液态水变成水蒸气 |
| C、弱酸弱碱电离 |
| D、用FeCl3饱和溶液制Fe(OH)3胶体 |
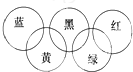 奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )
奥运会会标是五环旗,假定奥运五环旗中的一环表示一种物质,相连环物质间一定条件下能发生常见反应,不相连环物质间不能发生反应,且四种反应中必须包含化合反应、置换反应及复分解反应,适合的一组是( )