题目内容
2.已知X、Y、Z、R均为短周期元素,其中X与R为同族元素,且X的元素原子序数是R原子序数的2倍,X、Y处于同一周期,Y的原子半径是本周期元素原子中最大的,Z元素是所有元素中非金属性最强的元素.下列说法不正确的是( )| A. | 原子最外层电子数:Z>X=R>Y | |
| B. | Z与R形成的化合物中R显正价 | |
| C. | 离子半径:X2->Y+>R2->Z- | |
| D. | 四种元素中X元素形成的氢化物沸点最低 |
分析 已知X、Y、Z、R均为短周期元素,Z元素是所有元素中非金属性最强的元素,则Z为F元素;其中X与R为同族元素,且X的元素原子序数是R原子序数的2倍,则R为O元素,原子序数为8,X为S元素,原子序数为16;X、Y处于同一周期,则位于第三周期,Y的原子半径是本周期元素原子中最大的,所以Y为Na元素;结合元素周期律与元素化合物性质解答.
解答 解:已知X、Y、Z、R均为短周期元素,Z元素是所有元素中非金属性最强的元素,则Z为F元素;其中X与R为同族元素,且X的元素原子序数是R原子序数的2倍,则R为O元素,原子序数为8,X为S元素,原子序数为16;X、Y处于同一周期,则位于第三周期,Y的原子半径是本周期元素原子中最大的,所以Y为Na元素;
A.X为S元素,Y为Na元素,Z为F元素,R为O元素,则原子最外层电子数:Z>X=R>Y,故A正确;
B.化合物中电负性强的元素显负价,则F与O形成化合物中O显正价,故B正确;
C.电子层越多,离子半径越大,电子层相同时,原子序数越大,半径越小,则离子半径:S2->O2->F->Na+,故C错误;
D.四种元素形成的氢化物,NaHS为离子晶体,硫化氢、水和HF都是分子晶体沸点较低,其HF和水悠悠分子间存在氢键沸点高于硫化氢,所以S元素形成的氢化物沸点最低,故D正确.
故选C.
点评 本题考查结构性质位置关系、元素周期律等,难度不大,注意对元素周期律的理解以及掌握微粒半径比较,熟练掌握元素化合物性质与组成,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
10.下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A. | 10 mL 0.1 mol•L-1氨水与10 mL 0.1 mol•L-1盐酸混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) | |
| B. | 10 mL 0.1 mol•L-1NH4Cl溶液与5 mL 0.2 mol•L-1NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) | |
| C. | 10 mL 0.1 mol•L-1CH3COOH溶液与5 mL 0.2 mol•L-1NaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 10 mL 0.5 mol•L-1CH3COONa溶液与6 mL 1 mol•L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
10.在一定条件下,可逆反应A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A. | 单位时间内形成x mol的A-A键,同时形成x mol的A-B键 | |
| B. | 容器内的总压强不随时间变化,气体的密度不再随时间变化 | |
| C. | A2、AB、B2的浓度不再随时间改变 | |
| D. | 单位时间内生成x mol的A2分子,同时生成x mol的B2分子 |
17.短周期中的A、B、C、D、E五种元素,原子序数依次增大,A和D,C和E分别同主族,A为非金属元素,且A与B的原子序数之和等于C的原子序数,C2-与D+的核外电子数相等.则下列说法正确的是( )
| A. | B与A只能组成化合物BA3 | |
| B. | C、D、E形成的化合物与A、B、C形成的化合物可能发生氧化还原反应 | |
| C. | A2C2和D2C2具有完全相同类型的化学键 | |
| D. | E的最高价氧化物对应的水化物一定具有强的氧化性 |
12.下列说法中正确的是( )
| A. | NO2、SO2、BF3、NCl3分子中各原子均不满足最外层8电子结构 | |
| B. | 某化合物的焰色反应为黄色,则该化合物一定为钠盐 | |
| C. | NaCl晶体中与每个Na+距离相等且最近的Na+共有6个 | |
| D. | 单质的晶体中一定不存在的微粒是阴离子 |
 ;
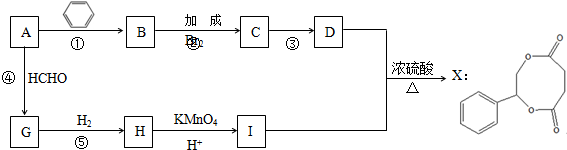
;
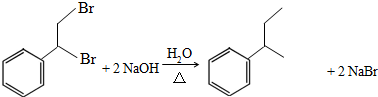 .
.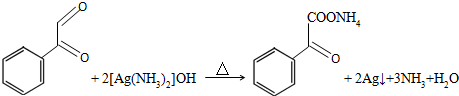 .
.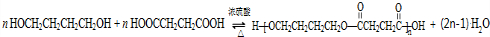 .
. 任意2种.
任意2种.
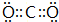 ,其中②原子的杂化方式为sp.
,其中②原子的杂化方式为sp.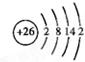 ,⑪原子的价电子排布式是4s24p3
,⑪原子的价电子排布式是4s24p3 由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,存在转化关系:甲$\stackrel{强酸溶液}{←}$丙$\stackrel{强碱溶液}{→}$乙
由短周期元素组成的甲、乙和丙均为中学常见物质,一定条件下,存在转化关系:甲$\stackrel{强酸溶液}{←}$丙$\stackrel{强碱溶液}{→}$乙