题目内容
14.利用有机物X可制取有机物Y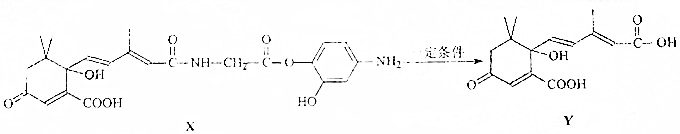
下列说法正确的是( )
| A. | X分子中有2个手性碳原子 | |
| B. | X可以发生酯化、加聚、缩聚反应,并能与盐酸反应生成有机盐 | |
| C. | 1molX与足量NaOH溶液反应,最多消耗5molNaOH | |
| D. | 1molY在一定条件下与H2发生加成反应,最多消耗5molH2 |
分析 A.连接四个不同原子或原子团的C原子为手性碳原子;
B.X中含有羰基、碳碳双键、羧基、醇羟基、肽键、酯基、酚羟基、氨基,具有酮、烯烃、羧酸、醇、二肽、酯、酚、胺的性质;
C.羧基、酯基水解生成的羧基和酚羟基、酚羟基、二肽水解生成的羧基都能和NaOH溶液反应;
D.Y中碳碳双键、羰基可与氢气发生加成反应.
解答 解:A.连有4个不同原子或原子团的碳原子为手性碳原子,则X中只有与-OH相连的C为手性碳原子,故A错误;
B.X中含有羰基、碳碳双键、羧基、醇羟基、肽键、酯基、酚羟基、氨基,具有酮、烯烃、羧酸、醇、二肽、酯、酚、胺的性质,所以能发生氧化、取代、酯化、加聚、缩聚反应,并能与盐酸反应生成有机盐,故B正确;
C.羧基、酯基水解生成的羧基和酚羟基、酚羟基、二肽水解生成的羧基都能和NaOH溶液反应,所以1mol X与足量NaOH溶液反应,最多消耗5mol NaOH,故C正确;
D.Y中碳碳双键、羰基可与氢气发生加成反应,则1molY在一定条件下与H2发生加成反应,最多消耗4molH2,故D错误.
故选BC.
点评 本题考查有机物的结构和性质,为高考常见题型,侧重于学生的分析能力的考查,注意把握有机物的结构特点和官能团的性质,为解答该题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.下列有关物质的性质与用途具有对应关系的是( )
| A. | 医用酒精能使蛋白质变性,可用于消毒杀菌 | |
| B. | SiO2有很好的折光率,可以用来做半导体材料 | |
| C. | 水玻璃易溶于水,可用于生产黏合剂和防火剂 | |
| D. | 氯化铝是强电解质,可电解其水溶液获得金属铝 |
5.铁屑和铜屑一起放入稀HNO3中,有少量铜屑剩余,则溶液中可能有的金属离子是( )
| A. | Fe3+和Cu2+ | B. | Fe2+和Cu2+ | C. | Fe2+和Fe3+ | D. | 只有Fe2+ |
2.体积为1L干燥容器中充入HCl气体后,测得容器中气体对氧气的相对密度为1.082(空气的平均摩尔质量为29g/mol).则容器中HCl气体的体积为( )
| A. | 0.25L | B. | 0.5L | C. | 0.75L | D. | 1L |
19.下列说法正确的是( )
| A. | 6.02×1023就是阿伏加德罗常数 | |
| B. | 1mol氧含 6.02×1023个 O2 | |
| C. | 1mol任何气体所含的气体分子数目都相等 | |
| D. | 摩尔是国际单位制中的一个基本物理量 |
6.对下列实验事实的解释或结论不正确的是( )
| 选项 | 操作、现象 | 解释或结论 |
| A | 向饱和Na2CO3溶液中通入少量CO2无浑浊出现 | 生成NaHCO3量少未使溶液饱和 |
| B | 用NaOH标准溶液滴定未知浓度盐酸,滴定终点时俯视读数 | 测定盐酸浓度偏低 |
| C | 向氯化钡溶液通入过量SO2无明显现象,再①通氯气②通氨气,两种操作均会产生白色沉淀 | 白色沉淀①为硫酸钡,②为亚硫酸钡 |
| D | 向1ml 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 在相同条件下,溶解度Mg(OH)2>Fe(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
3.下列有关叙述中不正确的是( )
| A. | 将SO2通入Ba(OH)2溶液中,有白色沉淀生成,加过量的稀盐酸后沉淀消失 | |
| B. | 将SO2通入BaCl2溶液中,有白色沉淀生成,加稀盐酸后沉淀消失 | |
| C. | 将SO2通入Ba(OH)2溶液中,有白色沉淀生成,加过量的稀硝酸后沉淀不消失 | |
| D. | 将SO2通入硝酸酸化的BaCl2溶液中,有白色沉淀生成,加稀盐酸后沉淀不消失 |



