题目内容
向2L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:
xA(g)+yB(g)?pC(g)+qD(g),已知:平均反应速率vC=
vA;反应2min时,A的浓度减少了
amol?L-1,B的物质的量减少了
mol,有a mol D生成.回答下列问题:
(1)反应2min内,vA= ,vB= ;
(2)该反应的化学方程式为 ;
(3)反应平衡时,D为2amol,则B的转化率为 (用a、b表示);
(4)反应平衡时,D为2amol,如果只升高反应温度,其他反应条件不变,平衡时D为1.5amol,则该反应的△H 0;(填“>”“<”或“=”).
xA(g)+yB(g)?pC(g)+qD(g),已知:平均反应速率vC=
| 1 |
| 2 |
| 1 |
| 6 |
| a |
| 2 |
(1)反应2min内,vA=
(2)该反应的化学方程式为
(3)反应平衡时,D为2amol,则B的转化率为
(4)反应平衡时,D为2amol,如果只升高反应温度,其他反应条件不变,平衡时D为1.5amol,则该反应的△H
考点:化学平衡的计算
专题:化学平衡专题
分析:已知:平均反应速率vC=
vA,根据化学反应速率之比等于化学计量数之比可知x:p=2:1,
反应2min时A的浓度减少了
mol/L,则A的物质的量减少了
mol,B的物质的量减少了
mol,有amolD生成,化学反应中,物质的物质的量变化量之比等于化学计量数之比,则x:y:q=
:
:a=2:3:6,
则x:y:p:q=2:3:1:6,即反应的化学方程式为2A(g)+3B(g)?C(g)+6D(g),
根据方程式计算相关物理量,结合影响化学平衡的因素解答该题.
| 1 |
| 2 |
反应2min时A的浓度减少了
| a |
| 6 |
| a |
| 3 |
| a |
| 2 |
| a |
| 3 |
| a |
| 2 |
则x:y:p:q=2:3:1:6,即反应的化学方程式为2A(g)+3B(g)?C(g)+6D(g),
根据方程式计算相关物理量,结合影响化学平衡的因素解答该题.
解答:
解:已知:平均反应速率vC=
vA,根据化学反应速率之比等于化学计量数之比可知x:p=2:1,
反应2min时A的浓度减少了
mol/L,则A的物质的量减少了
mol,B的物质的量减少了
mol,有amolD生成,化学反应中,物质的物质的量变化量之比等于化学计量数之比,则x:y:q=
:
:a=2:3:6,
则x:y:p:q=2:3:1:6,即反应的化学方程式为2A(g)+3B(g)?C(g)+6D(g),
(1)VA=
mol/(L?min)=
mol/(L?min),VB=
VA=
×
mol/(L?min)=
mol/(L?min);
故答案为:
mol/(L?min),
mol/(L?min);
(2)由以上分析可知x:y:p:q=2:3:1:6,则x=2,p=1,则x:y:p:q=2:3:1:6,即反应的化学方程式为:2A(g)+3B(g)?C(g)+6D(g),
故答案为:2A(g)+3B(g)?C(g)+6D(g);
(3)反应达到平衡时,D为2amol,由方程式2A(g)+3B(g)?C(g)+6D(g)可知消耗的B为amol,则B的转化率为
×100%;
故答案为:
×100%;
(4)由(3)知平衡时D为2amol,如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,说明升高温度平衡向逆反应方向移动,则正反应放热,即△H<0,
故答案为:<.
| 1 |
| 2 |
反应2min时A的浓度减少了
| a |
| 6 |
| a |
| 3 |
| a |
| 2 |
| a |
| 3 |
| a |
| 2 |
则x:y:p:q=2:3:1:6,即反应的化学方程式为2A(g)+3B(g)?C(g)+6D(g),
(1)VA=
| ||
| 2min |
| a |
| 12 |
| 3 |
| 2 |
| 3 |
| 2 |
| a |
| 12 |
| a |
| 8 |
故答案为:
| a |
| 12 |
| a |
| 8 |
(2)由以上分析可知x:y:p:q=2:3:1:6,则x=2,p=1,则x:y:p:q=2:3:1:6,即反应的化学方程式为:2A(g)+3B(g)?C(g)+6D(g),
故答案为:2A(g)+3B(g)?C(g)+6D(g);
(3)反应达到平衡时,D为2amol,由方程式2A(g)+3B(g)?C(g)+6D(g)可知消耗的B为amol,则B的转化率为
| a |
| b |
故答案为:
| a |
| b |
(4)由(3)知平衡时D为2amol,如果只升高反应温度,其他反应条件不变,平衡时D为1.5a mol,说明升高温度平衡向逆反应方向移动,则正反应放热,即△H<0,
故答案为:<.
点评:本题考查化学平衡的计算,题目难度中等,根据反应速率关系以及物质的量的转化关系判断反应的化学方程式是解答该题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列离子方程式书写不正确的是( )
| A、CuSO4溶液吸收H2S气体 Cu2++H2S=CuS↓+2H+ |
| B、NH4HSO4溶液中加入等物质的量的Ba(OH)2 溶液NH4++H++SO42-+Ba2++2OH-=NH3?H2O+BaSO4↓+H2O |
| C、向NaAlO2溶液中通入过量CO2制Al(OH)3AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| D、氧化铁溶于氢碘酸 Fe2O3+6H+=2Fe3++3H2O |
对于反应2SO2(g)+O2(g)?2SO3(g),能增大正反应速率且提高O2的转化率的措施是( )
| A、移去部分SO3 |
| B、降低体系温度 |
| C、通入大量O2 |
| D、通入大量SO2 |
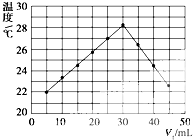 将V1 mL 1.00mol?L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )
将V1 mL 1.00mol?L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).下列叙述正确的是( )| A、做该实验时环境温度为22℃ |
| B、该实验表明所有化学反应化学能只转化为热能 |
| C、NaOH溶液的浓度为1.50 mol?L-1 |
| D、该实验表明有水生成的反应都是放热反应 |