��Ŀ����
����ij�¶���ƽ����ϵmA(g) + nB(g) pC(g) + qD(g) ��H<0������˵������ȷ����
pC(g) + qD(g) ��H<0������˵������ȷ����
A�����¶Ȳ��佫�����ݻ�����ԭ����2������ʱA��Ũ�ȱ�Ϊԭ����0.52������m + n > p + q
B����ƽ����ϵ�м���C��D���÷�Ӧ�ġ�H��С
C�����¶Ⱥ�����������䣬����һ�����Ķ������壬B��Ũ�Ȳ���
D����ƽ��ʱ������A������A��ת�����½���B��ת��������
B
��������
���������A�����¶Ȳ��佫�����ݻ�����ԭ����2������ƽ�ⲻ�ƶ�����A��Ũ�ȱ�Ϊԭ����0.5������ʱA��Ũ�ȱ�Ϊԭ����0.52����˵���������ѹǿ��С��ƽ�������ƶ������������������ʵ�������ķ�������m+n>p+q����ȷ��B����Ӧ�������ʵ�״̬������ʽ�з�Ӧ���ϵ���йأ���ʵ�ʷ�Ӧ�����ʵ����أ����Ը÷�Ӧ�ġ�H���䣬����C�����¶Ⱥ�����������䣬����һ�����Ķ������壬����Ӧ��ϵ�и����ʵ�Ũ�Ⱦ����䣬����ƽ�ⲻ�ƶ���B��Ũ�Ȳ��䣬��ȷ��D�����ڶ��ַ�Ӧ��ķ�Ӧ������һ�����ʵ������������������ʵ�ת���ʣ���������ת���ʽ��ͣ�����ƽ��ʱ������A������A��ת�����½���B��ת�������ӣ���ȷ����ѡB��
���㣺����������ƽ���ƶ���Ӱ��

��10�֣����³�ѹ�£�����1mol������ӻ�ѧ�������յ��������γ�1mol������ӻ�ѧ�����ų���������Ϊ���ܣ���λΪkJ.mol-1���������±��������ݣ�kJ��mol��1���ش����⣺
��ѧ�� | C��F | C��Cl | C��I | H��H | S��S | H��S |
���� | 427 | 330 | 218 | 436 | 255 | 339 |
��1���ɱ�������Ԥ��C��Br���ļ��ܷ�Χ��_________��C��Br���ܣ�_________���ش���ֵ�͵�λ��
��2���Ȼ�ѧ����ʽ2H2(g)��S2(g) = 2H2S(g)����H= QkJ��mol��1����Q=
��3����֪�����Ȼ�ѧ����ʽ��
��O2 (g) = O+2(g) + e- 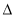 H1= +1175.7 kJ��mol-1 ��PtF6(g) + e- = PtF6��(g)
H1= +1175.7 kJ��mol-1 ��PtF6(g) + e- = PtF6��(g) 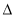 H2= -771.1 kJ��mol-1
H2= -771.1 kJ��mol-1
��O2+PtF6-(s) = O2+(g) + PtF6-(g)  H3= +482.2 kJ��mol-1
H3= +482.2 kJ��mol-1
��ӦO2(g) + (g) = O2+PtF6-(s) 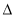 H=_____________ kJ��mol-1��
H=_____________ kJ��mol-1��
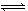 2NO+O2�ں��º����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־��
2NO+O2�ں��º����ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�� 2 NH3 (g)��ƽ����ϵ��,������������,���ӵ�����Ũ��,�����ж���ȷ����
2 NH3 (g)��ƽ����ϵ��,������������,���ӵ�����Ũ��,�����ж���ȷ����