题目内容
潮湿的氯气、新制的氯水、次氯酸钠及漂白粉的水溶液均能使有色布条褪色,是因为它们均含有( )
| A、氯气 | B、次氯酸 |
| C、次氯酸根 | D、盐酸 |
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:潮湿的氯气,新制的氯水,次氯酸钠溶液及漂白粉的水溶液均由漂白性,最终产生漂白作用的物质是次氯酸.
解答:
解:氯气、盐酸均不具有漂白性,潮湿的氯气,新制的氯水,次氯酸钠溶液及漂白粉的水溶液中均含有次氯酸,次氯酸能使有色布条褪色.
故选B.
故选B.
点评:本题考查学生次氯酸的漂白性知识,为高频考点,侧重于化学与生活的考查,注意次氯酸盐的漂白原理最终也是生成次氯酸的缘故,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知吡啶(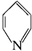 )与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是
)与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是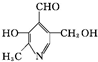 +H3PO4
+H3PO4
H2O+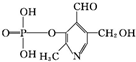 磷酸吡醛( )
磷酸吡醛( )
 )与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是
)与苯环性质相似.有机物M与磷酸在一定条件下形成磷酸吡醛,磷酸吡醛是细胞的重要组成部分.下列说法不正确的是 +H3PO4
+H3PO4| 一定条件 |
 磷酸吡醛( )
磷酸吡醛( )| A、M能使酸性高锰酸钾溶液褪色 |
| B、1 mol M能与金属钠反应,消耗2 mol Na |
| C、1 mol磷酸吡醛与NaOH溶液反应,最多消耗3 mol NaOH |
| D、M与足量H2反应后所得有机物的分子式为C8H17O3N |
在一定的温度下,可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A、A、B、C的分子数相等 |
| B、A、B、C的浓度相等 |
| C、单位时间生成n mol A,同时生成2n mol C |
| D、A、B、C的分子数之比为1:3:2 |
赤铜矿的成分是Cu2O,辉铜矿的成分是Cu2S,将赤铜矿与辉铜矿混合加热有以下反应:Cu2S+2Cu2O
6Cu+SO2↑;对于该反应的下列说法正确的是( )
| △ |
| A、该反应中的氧化剂只有Cu2O |
| B、Cu2S在反应中既是氧化剂又是还原剂 |
| C、Cu既是氧化产物又是还原产物 |
| D、氧化产物与还原产物的物质的量之比为1:6 |
下列各组中的离子,能在无色酸性溶液中大量共存的是( )
| A、Na+、Mg2+、Cl-、HCO3- |
| B、K+、Cu2+、SO42-、NO3- |
| C、K+、Na+、OH-、Cl- |
| D、Mg2+、Al3+、NO3-、SO42- |