题目内容
6.在一密闭容器中,反应 aA(g)?bB(g)达到平衡后,保持温度不变,将容器体积增大一倍,达到新的平衡时,B的浓度是原来的40%,则下列说法正确的是( )
| A. | 平衡向正反应方向移动了 | B. | 物质A的转化率增加了 | ||
| C. | 物质B的质量分数减少了 | D. | b>a |
分析 采用假设法分析,假设a=b,保持温度不变,将容器体积增加一倍,平衡不移动,A和B的浓度应均是原来的$\frac{1}{2}$倍,与达到新的平衡时B的浓度相比判断平衡移动,保持温度不变,将容器体积增大一倍,达到新的平衡时,B的浓度是原来的40%,说明压强减小平衡逆向进行,再根据平衡移动逐项判断.
解答 解:采用假设法分析,假设a=b,保持温度不变,将容器体积增加一倍,平衡不移动,A和B的浓度应均是原来的$\frac{1}{2}$倍,但当达到新的平衡时,B的浓度是原来的40%,说明减小压强平衡向逆反应反应方向移动,
A、平衡时B的浓度是原来的40%,小于原来的$\frac{1}{2}$倍,说明平衡向逆反应反应方向移动,故A错误;
B、平衡时B的浓度是原来的40%,小于原来的$\frac{1}{2}$倍,说明平衡向逆反应反应方向移动,A的转化率减小,故B错误;
C、平衡应向逆反应方向移动,物质B的质量减小,混合物总质量不变,所以物质B质量分数减小,故C正确;
D、增大体积,压强减小,平衡向逆反应方向移动,压强减小平衡向气体体积增大的方向进行,则说明a>b,故D错误.
故选C.
点评 本题考查化学平衡移动影响因素,化学平衡移动原理的理解应用,题目难度不大,注意通过改变体积,物质的浓度的变化判断平衡移动的方向,此为解答该题的关键.

练习册系列答案
相关题目
7.下列实验能达到预期目的是( )
| A. | 向淀粉溶液中加入稀硫酸,加热一段时间后再加入银氨溶液,水浴加热,检验淀粉是否水解 | |
| B. | 向甲酸和甲醛的混合物中加入氢氧化钠溶液,中和甲酸后,加入新制的氢氧化铜加热,检验混合物中是否含有甲醛 | |
| C. | 制硝基苯时,将盛有混合液的试管加热,控制温度100-110℃ | |
| D. | 要鉴别己烯中是否混有甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 |
8.在CO2的水溶液中,H2CO3达到电离平衡的标志是( )
| A. | c(HCO3-)=c(CO32-) | B. | 溶液中无H2CO3 | ||
| C. | c(HCO3-)恒定不变 | D. | 溶液中H2CO3、HCO3-、CO32-共存 |
5.等体积的pH=12的碱溶液甲和pH=11的碱溶液乙,分别用等浓度的盐酸中和时,消耗盐酸的体积为2V甲=V乙,下列判断合理的是( )
| A. | 乙一定是弱碱 | B. | 甲一定是强碱 | C. | 乙一定是二元碱 | D. | 甲一定是一元碱 |
11.下列解释实验事实的方程式不准确的是( )
| A. | 0.1 mol•L-1 CH3COOH溶液的pH>1:CH3COOH?CH3COO-+H+ | |
| B. | “NO2球”浸泡在冷水中,颜色变浅:2NO2(g)???N2O4(g)△H<0 (红棕色) (无色) | |
| C. | 铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO${\;}_{3}^{-}$═3Fe3++2NO↑+4H2O | |
| D. | 向Na2CO3溶液中滴入酚酞溶液,溶液变红:CO${\;}_{3}^{2-}$+H2O?HCO${\;}_{3}^{-}$+OH- |
16.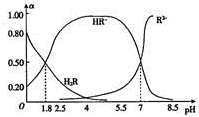 室温时,0.1mol.L-1二元弱酸HzR溶液中H2R、HR-、R2-三种微粒所占物质的量分数(a)随pH的变化趋势如图所示.下列说法不正确的是( )
室温时,0.1mol.L-1二元弱酸HzR溶液中H2R、HR-、R2-三种微粒所占物质的量分数(a)随pH的变化趋势如图所示.下列说法不正确的是( )
 室温时,0.1mol.L-1二元弱酸HzR溶液中H2R、HR-、R2-三种微粒所占物质的量分数(a)随pH的变化趋势如图所示.下列说法不正确的是( )
室温时,0.1mol.L-1二元弱酸HzR溶液中H2R、HR-、R2-三种微粒所占物质的量分数(a)随pH的变化趋势如图所示.下列说法不正确的是( )| A. | H2R的一级电离平衡常数Kal≈0.25 | |
| B. | pH=2.5的H2R溶液中:c(HR-)+2c(R2-)+c(OH-)=l0-2.5 | |
| C. | pH=5.5的该溶液中:c(HR一)>c(R2一)>c(H+)>c(OH一) | |
| D. | 向pH=7的该溶液中滴加少量稀硫酸,a(HR-)减小 |