题目内容
一定条件下,将一定量的气体A和气体B通入密闭恒容的容器中,发生反应 2A(g) + 3B(g) 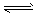 3C (g ) ,下列说法中,能够说明该反应达到平衡状态的是
3C (g ) ,下列说法中,能够说明该反应达到平衡状态的是
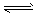 3C (g ) ,下列说法中,能够说明该反应达到平衡状态的是
3C (g ) ,下列说法中,能够说明该反应达到平衡状态的是 [ ]
A.各物质的浓度之比为C(A) :C(B) : C(C) =2:3:3
B.气体的总体积是反应开始时的3/5
C.混合气体的密度不变
D.单位时间内,若消耗了a mol A,同时也消耗了1.5 a mol C
B.气体的总体积是反应开始时的3/5
C.混合气体的密度不变
D.单位时间内,若消耗了a mol A,同时也消耗了1.5 a mol C
D

练习册系列答案
相关题目
 一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
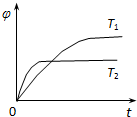
一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:m A(s)+n B(g)═p C(g)+q D(g)△H 达到平衡后,测得B的浓度为0.5mol/L.保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后,测得B的浓度为0.3mol?L-1.当其它条件不变时,C在反应混合物中的体积分数(φ)与温度(T)、时间(t)的关系如图所示.下列叙述正确的是( )
| A、热化学方程式中:n<p+q | B、热化学方程式中:△H>0 | C、达平衡后,增加A的量,有利于提高B的转化率 | D、若T1、T2时反应的平衡常数分别为K1、K2,则K1>K2 |
 (2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应:
(2011?崇文区模拟)一定条件下,将一定量的A、B、C、D四种物质,置于密闭容器中发生如下反应: p C(g)+q D(g)达到平衡后,测得B的浓度为0.5
p C(g)+q D(g)达到平衡后,测得B的浓度为0.5 p C(g)+q D(g) △H
p C(g)+q D(g) △H )与温度(T)、时间(t)的关系如下图所示。下列叙述正确的是( )
)与温度(T)、时间(t)的关系如下图所示。下列叙述正确的是( )