题目内容
14.室温下,柠檬水溶液的pH是3,其中c(OH-)是( )| A. | 1×10-11mol/L | B. | 1×10-3mol/L | C. | 1×10-7mol/L | D. | 0.1mol/L |
分析 pH=3的柠檬水溶液中氢离子浓度为1×10-3mol/L,根据c(OH-)=$\frac{1×1{0}^{-14}}{c({H}^{+})}$计算出该溶液中氢氧根离子浓度.
解答 解:室温下,柠檬水溶液的pH是3,该溶液中氢离子浓度为1×10-3mol/L,根据c(OH-)=$\frac{1×1{0}^{-14}}{c({H}^{+})}$=$\frac{1×1{0}^{-14}}{1×1{0}^{-3}}$mol/L=1×10-11mol/L,
故选A.
点评 本题考查了溶液pH的简单计算,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,注意掌握pH的概念及表达式,试题培养了学生的化学计算能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列说法不正确的是( )
| A. | 熵增加且放热的反应一定是自发反应 | |
| B. | X?Y+Z正反应吸热,则逆反应必然放热 | |
| C. | 化学反应的焓变△H越大,表示放热越多 | |
| D. | 稀溶液中,酸碱中和反应生成1 mol H2O时放热不一定为57.3 kJ |
9.下列两种溶液混合后,所得溶液中各离子浓度关系不正确的是( )
| A. | 0.1 mol/L的NaOH溶液与0.1 mol/L的CH3COOH溶液等体积混合c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| B. | 常温下,0.01 mol/L的NaOH溶液与pH=2的CH3COOH溶液等体积混合c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | 常温下,0.1 mol/L的CH3COOH溶液与0.1 mol/L的NaOH溶液混合后使pH=7,c(CH3COO-)=c(Na+)>c(H+)=c(OH-) | |
| D. | 0.1 mol/L的CH3COOH溶液和0.1 mol/L的CH3COONa溶液等体积混合c(CH3COO-)+c(OH-)=c(Na+)+c(H+) |
6.下列物质属于酚类的是( )
| A. | 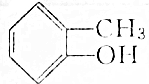 | B. | 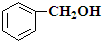 | ||
| C. | 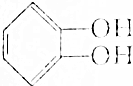 | D. | 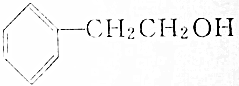 |
3.苹果汁中含有Fe2+,现榨的苹果汁在空气中会由浅绿色变为棕黄色.若榨汁时加入维生素C,可有效防止这种现象发生.这说明维生素C具有( )
| A. | 氧化性 | B. | 还原性 | C. | 碱性 | D. | 酸性 |
4.现有①NaHCO3、②Al、③Al2O3、④Al(OH)3、⑤AlCl3五种物质,其中既能与盐酸反应又能与NaOH溶液反应的是( )
| A. | ②③④⑤ | B. | ①③④ | C. | ①②③④ | D. | 全部 |