题目内容
请按下列要求写出有关反应的离子方程式:
(1)铜与氯化铁的反应
(2)往氯化亚铁中通入氯气
(3)①向10L0.1mol?L-1的NaHCO3溶液中滴入含有 0.5mol Ba(OH)2的溶液.写出反应的离子方程式 .
②向所得溶液中加入等体积同浓度的Ba(OH)2溶液.写出此步反应的离子方程式 .
(1)铜与氯化铁的反应
(2)往氯化亚铁中通入氯气
(3)①向10L0.1mol?L-1的NaHCO3溶液中滴入含有 0.5mol Ba(OH)2的溶液.写出反应的离子方程式
②向所得溶液中加入等体积同浓度的Ba(OH)2溶液.写出此步反应的离子方程式
考点:离子方程式的书写
专题:离子反应专题
分析:(1)铜与氯化铁发生氧化还原反应生成氯化铜和氯化亚铁;
(2)氯化亚铁中二价铁离子具有还原性,通入氯气被氧化为氯化铁;
(3)①NaHCO3与Ba(OH)2 按照物质的量之比2:1反应生成碳酸钡、碳酸钠和水;
②反应生成的碳酸钠与氢氧化钡发生复分解反应生成碳酸钡沉淀和氢氧化钠.
(2)氯化亚铁中二价铁离子具有还原性,通入氯气被氧化为氯化铁;
(3)①NaHCO3与Ba(OH)2 按照物质的量之比2:1反应生成碳酸钡、碳酸钠和水;
②反应生成的碳酸钠与氢氧化钡发生复分解反应生成碳酸钡沉淀和氢氧化钠.
解答:
解:(1)铜与氯化铁发生氧化还原反应生成氯化铜和氯化亚铁,离子方程式为:Cu+2Fe3+═Cu2++2Fe2+,
故答案为:Cu+2Fe3+═Cu2++2Fe2+;
(2)氯化亚铁中通入氯气反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,
故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(3)①NaHCO3与Ba(OH)2 按照物质的量之比2:1反应生成碳酸钡、碳酸钠和水,反应的离子方程式为:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O,
故答案为:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O;
②碳酸钠与氢氧化钡发生复分解反应生成碳酸钡沉淀和氢氧化钠,反应的离子方程式为:Ba2++CO32-═BaCO3↓,
故答案为Ba2++CO32-═BaCO3↓.
故答案为:Cu+2Fe3+═Cu2++2Fe2+;
(2)氯化亚铁中通入氯气反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,
故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(3)①NaHCO3与Ba(OH)2 按照物质的量之比2:1反应生成碳酸钡、碳酸钠和水,反应的离子方程式为:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O,
故答案为:Ba2++2HCO3-+2OH-═BaCO3↓+CO32-+2H2O;
②碳酸钠与氢氧化钡发生复分解反应生成碳酸钡沉淀和氢氧化钠,反应的离子方程式为:Ba2++CO32-═BaCO3↓,
故答案为Ba2++CO32-═BaCO3↓.
点评:本题考查了离子方程式的书写,题目难度不大,正确书写出反应的离子方程式,然后依据化学式拆分的原则改写成离子方程式即可,(3)为易错点.

练习册系列答案
相关题目
设NA为阿伏伽德罗常数,下列说法中正确的是( )
| A、7.8g过氧化钠固体中含阴离子个数为0.2NA |
| B、34g氨气中含N-H的数目为6NA |
| C、标准状况下,22.4L乙炔中含π键数为2NA |
| D、1molNaHSO4晶体中阳离子数为2NA |
下列反应属于吸热反应的是( )
| A、稀硫酸与氢氧化钾溶液反应 |
| B、氢氧化钡晶体与氯化铵晶体研磨搅拌的反应 |
| C、锌与稀硫酸的反应 |
| D、生石灰变成熟石灰的反应 |
如图是立方烷的球棍模型,下列有关说法不正确的是( )
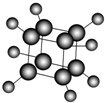

| A、其一氯代物只有一种 |
| B、其二氯代物有三种 |
| C、分子中σ键均由sp3-s电子云重叠而成 |
| D、它与苯乙烯(C6H5-CH=CH2)互为同分异构体 |
下列有关物理量相应的单位表达中,错误的是( )
| A、气体摩尔体积L/g |
| B、摩尔质量g/mol |
| C、物质的量浓度mol/L |
| D、物质的量 mol |