题目内容
下列各种离子一定能大量共存的是( )
| A、强碱性溶液中:Na+、K+、AlO2-、CO32- |
| B、含有大量Fe3+的溶液中:NH4+、SCN-、Cl-、K+ |
| C、在与铝产生氢气的溶液中:NH4+、K+、SO42-、HCO3- |
| D、在使石蕊变红的溶液中:K+、Fe2+、Cl-、NO3- |
考点:离子共存问题
专题:离子反应专题
分析:A.强碱性溶液中存在大量氢氧根离子,Na+、K+、AlO2-、CO32-离子之间不发生反应,也不与氢氧根离子反应;
B.铁离子与硫氰根离子反应生成络合物硫氰化铁;
C.在与铝产生氢气的溶液中存在大量氢离子或者氢氧根离子,铵根离子、碳酸氢根离子能够与氢氧根离子反应,碳酸氢根离子与氢离子反应;
D.使石蕊变红的溶液为酸性溶液,硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子.
B.铁离子与硫氰根离子反应生成络合物硫氰化铁;
C.在与铝产生氢气的溶液中存在大量氢离子或者氢氧根离子,铵根离子、碳酸氢根离子能够与氢氧根离子反应,碳酸氢根离子与氢离子反应;
D.使石蕊变红的溶液为酸性溶液,硝酸根离子在酸性条件下具有强氧化性,能够氧化亚铁离子.
解答:
解:A.强碱性溶液中存在大量OH-,Na+、K+、AlO2-、CO32-离子之间不反应,且都不与氢氧根离子反应,在 溶液中能够大量共存,故A正确;
B.Fe3+、SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.在与铝产生氢气的溶液中存在大量H+或OH-,NH4+、HCO3-离子与氢氧根离子反应,HCO3-离子与与氢原子反应,在溶液中不能大量共存,故C错误;
D.使石蕊变红的溶液中存在大量H+,:K+、Cl-、NO3-离子在酸性条件下能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选A.
B.Fe3+、SCN-之间反应生成硫氰化铁,在溶液中不能大量共存,故B错误;
C.在与铝产生氢气的溶液中存在大量H+或OH-,NH4+、HCO3-离子与氢氧根离子反应,HCO3-离子与与氢原子反应,在溶液中不能大量共存,故C错误;
D.使石蕊变红的溶液中存在大量H+,:K+、Cl-、NO3-离子在酸性条件下能够氧化Fe2+,在溶液中不能大量共存,故D错误;
故选A.
点评:本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等.

练习册系列答案
相关题目
已知:CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-Q1 kJ?mol-1
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H=-Q2 kJ?mol-1
上述均是在溶液中进行的反应,Q1、Q2的关系正确的是( )
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(l)△H=-Q2 kJ?mol-1
上述均是在溶液中进行的反应,Q1、Q2的关系正确的是( )
| A、Q1=Q2=57.3 |
| B、Q1>Q2>57.3 |
| C、Q1<Q2=57.3 |
| D、无法确定 |
下列装置中电流表指针会发生偏转的是( )
A、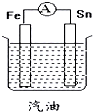 |
B、 |
C、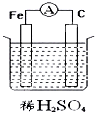 |
D、 |
已知:HCl为强酸,下列对比实验不能用于证明CH3COOH为弱酸的是( )
| A、对比等浓度的两种酸的pH |
| B、对比等浓度的两种酸,与相同大小镁条反应的初始速率 |
| C、对比等浓度、等体积的两种酸,与等量NaOH溶液反应后放出的热量 |
| D、对比等浓度、等体积的两种酸,与足量Zn反应,生成H2的体积 |
下列有关金属腐蚀与防护的说法正确的是( )
| A、可将地下输油管与外加直流电源的正极相连以保护它不受腐蚀 |
| B、当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C、在海轮外壳连接一锌块保护外壳不受腐蚀是采用了牺牲阴极的阳极保护法 |
| D、纯银器表面在空气中因化学腐蚀渐渐变暗 |
一种新型燃料电池,它是用惰性金属作电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气,发生的电极反应为:X极:CH4+10OH--8e-=CO32-+7H2O Y极:2O2+4H2O+8e-=8OH-;关于此燃料电池的说法不正确的是( )
| A、该电池工作时通甲烷一极附近溶液的pH升高 |
| B、工作一段时间后,KOH的物质的量减少 |
| C、X极发生氧化反应,Y极发生还原反应 |
| D、在标准状况下通入5.6 L O2完全反应,则有1 mol电子发生转移 |
 某研究性学习小组用如图所示装置研究不同能量之间的转化问题.下列说法正确的是( )
某研究性学习小组用如图所示装置研究不同能量之间的转化问题.下列说法正确的是( )| A、断开开关S1,按下开关S2,此时构成的装置属于电解池 |
| B、断开开关S1,按下开关S2,化学能转化为电能,电能转化为光能等 |
| C、断开开关S2,按下开关S1,此时构成的装置属于原电池 |
| D、断开开关S2,按下开关S1,化学能转化为电能 |
下列说法中不正确是( )
| A、为保护地下钢管不受腐蚀,可使它与直流电源正极相连 |
| B、生铁比纯铁易生锈 |
| C、钢铁发生电化腐蚀比化学更普遍 |
| D、钢铁发生电化腐蚀时其负极反应为;Fe-2e-═Fe2+ |
下列关于焓变的叙述中正确的是( )
| A、化学反应的焓变与反应的方向性无关 |
| B、化学反应的焓变直接决定了反应的方向 |
| C、焓变为正的反应都是吸热反应 |
| D、焓变为负的反应都能自发进行 |