题目内容
(5分)卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的___________区;
(2)氟的电子排布图为___________________;
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是______________;

(4)已知碘酸HIO3和高碘酸H5IO6的结构分别如图I、图II所示:

请比较二者酸性强弱:HIO3_________H5IO6(填“>”“<”或“=”);
(5)下图为碘晶体晶胞结构。下列说法中正确的是_________.

A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以8配位数交替配位形成层状结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(1)p (2)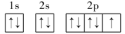 (3)碘 (4)> (5)D
(3)碘 (4)> (5)D
【解析】
试题分析:(1)卤族元素位于元素周期表的第17纵行,属于p区;(2)9号元素氟的电子排布图为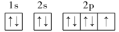 ;(3)元素的原子的第一电离能越小,则原子越容易失去电子,形成单核阳离子的可能性就越大,所以根据元素的第一电离能的大小数据可知:碘元素的第一电离能最小,所以碘元素最有可能生成较稳定的单核阳离子;(4)碘酸HIO3是中强酸,而高碘酸H5IO6则是五元弱酸,所以酸性:HIO3>H5IO6;(5)A.碘分子的排列有2种不同的取向,每个碘分子的配位数是(3×8)÷2=12,错误;B.用均摊法可知平均每个晶胞中有的碘分子个数是:(8×1/8)+6×1/2=4个,所以含有8个碘原子,错误;C.碘晶体为分子晶体,不是原子晶体,错误;D.由于碘分子是单质分子,所以在碘晶体中存在的相互作用有非极性键和范德华力,正确。
;(3)元素的原子的第一电离能越小,则原子越容易失去电子,形成单核阳离子的可能性就越大,所以根据元素的第一电离能的大小数据可知:碘元素的第一电离能最小,所以碘元素最有可能生成较稳定的单核阳离子;(4)碘酸HIO3是中强酸,而高碘酸H5IO6则是五元弱酸,所以酸性:HIO3>H5IO6;(5)A.碘分子的排列有2种不同的取向,每个碘分子的配位数是(3×8)÷2=12,错误;B.用均摊法可知平均每个晶胞中有的碘分子个数是:(8×1/8)+6×1/2=4个,所以含有8个碘原子,错误;C.碘晶体为分子晶体,不是原子晶体,错误;D.由于碘分子是单质分子,所以在碘晶体中存在的相互作用有非极性键和范德华力,正确。
考点:考查卤素在周期表中的位置、原子的电子排布图、物质酸性强弱的比较、均摊法在晶体中的应用。

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
 、
、 、
、 表示。已知: 2
表示。已知: 2