题目内容
NA代表阿伏加德罗常数,下列说法中正确的是( )
| A、标况下,11.2 L氯气完全溶于1 L水中,所得溶液中Cl-和ClO-两种粒子数之和为NA |
| B、80mL 10mol?L-1 盐酸与足量MnO2加热反应,产生Cl2分子数为0.2NA |
| C、含有4 NA个碳碳σ键的金刚石,其质量为24 g |
| D、含0.1 mol FeCl3的溶液完全水解后得到的胶体粒子个数为0.1 NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氯气溶于水,只有部分氯气与水反应生成氯化氢和次氯酸,则氯水中存在氯离子、次氯酸根离子和氯气,Cl-和ClO-两种粒子的物质的量小于1mol;
B.浓盐酸变成稀盐酸后,反应停止,反应生成的氯气减少;
C.1mol金刚石含有2NA个碳碳σ键,4NA个碳碳σ键的金刚石2mol;
D.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算胶体中含有的胶粒数目.
B.浓盐酸变成稀盐酸后,反应停止,反应生成的氯气减少;
C.1mol金刚石含有2NA个碳碳σ键,4NA个碳碳σ键的金刚石2mol;
D.氢氧化铁胶粒为氢氧化铁的聚集体,无法计算胶体中含有的胶粒数目.
解答:
解:A.标况下11.2L氯气的物质的量为0.5mol,由于氯气与水反应为可逆反应,溶液中还存在氯气分子,所得溶液中Cl-和ClO-两种粒子数之和小于NA,故A错误;
B.80mL 10mol?L-1盐酸中含有0.8mol氯化氢,消耗0.8mol氯化氢能够生成0.2mol氯气,由于随着反应的进行,浓盐酸会变成稀盐酸,反应停止,则反应生成的氯气小于0.2mol,产生氯气的分子数小于0.2NA,故B错误;
C.1mol金刚石含有2NA个碳碳σ键,4NA个碳碳σ键的金刚石2mol,质量为24g,故C正确;
D.水解不可能完全,水解是微弱的,且氢氧化铁胶粒为氢氧化铁的聚集体,所以0.1mol FeCl3的溶液完全水解后得到的胶体粒子个数小于0.1NA,故D错误;
故选C.
B.80mL 10mol?L-1盐酸中含有0.8mol氯化氢,消耗0.8mol氯化氢能够生成0.2mol氯气,由于随着反应的进行,浓盐酸会变成稀盐酸,反应停止,则反应生成的氯气小于0.2mol,产生氯气的分子数小于0.2NA,故B错误;
C.1mol金刚石含有2NA个碳碳σ键,4NA个碳碳σ键的金刚石2mol,质量为24g,故C正确;
D.水解不可能完全,水解是微弱的,且氢氧化铁胶粒为氢氧化铁的聚集体,所以0.1mol FeCl3的溶液完全水解后得到的胶体粒子个数小于0.1NA,故D错误;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确氢氧化铁胶粒为氢氧化铁的聚集体,熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意浓盐酸与二氧化锰的反应中,浓盐酸变成稀盐酸后反应停止.

练习册系列答案
相关题目
下列变化需要加入还原剂才能实现的是( )
| A、Fe3+→Fe2+ |
| B、HCl→Cl2 |
| C、Fe→Fe2+ |
| D、Na→Na2O |
下列化学用语的表达正确的是( )
A、氯原子的核外电子排布图: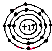 |
B、氮气分子的电子式: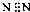 |
| C、乙炔分子的结构式:CH≡CH |
D、CH4分子的比例模型: |
在1828年,德国化学键Wohler通过蒸发一种无机盐的水溶液,得到了有机物尿素CO(NH2)2.这一成果被称为有机化学发展史上的里程碑,Wohler使用的无机盐是( )
| A、NH4CNO |
| B、(NH4)2CO3 |
| C、CH3COONH4 |
| D、NH4NO3 |
用NA表示阿伏伽德罗常熟的值,下列叙述正确的是( )
| A、标准状况下,22.4LH2O含有的原子总数为3NA |
| B、常温常压下,含有NA个氖原子的氖气体积约为22.4L |
| C、4g金属钙变成钙离子时失去的电子数目为0.1NA |
| D、2L0.5mol?L-1的氯化镁溶液中所含的离子总数为3NA |