题目内容
如图是四种常见有机物的比例模型示意图.下列说法不正确的是( )

| A、甲能使酸性高锰酸钾溶液褪色 |
| B、乙能与溴水发生加成反应使溴水褪色 |
| C、丙分子中所有原子均在同一平面上 |
| D、丁在浓硫酸作用下可与乙酸发生取代反应 |
考点:有机物的结构和性质,有机物分子中的官能团及其结构
专题:有机化学基础
分析:由四种有机物的比例模型可知,甲为甲烷,乙为乙烯,丙为苯,丁为乙醇.
A.甲烷为饱和烃,与高锰酸钾不反应;
B.乙烯中含双键;
C.苯环为平面结构;
D.乙醇中含-OH,可发生酯化反应.
A.甲烷为饱和烃,与高锰酸钾不反应;
B.乙烯中含双键;
C.苯环为平面结构;
D.乙醇中含-OH,可发生酯化反应.
解答:
解:由四种有机物的比例模型可知,甲为甲烷,乙为乙烯,丙为苯,丁为乙醇.
A.甲烷为饱和烃,与高锰酸钾不反应,则不能使酸性高锰酸钾溶液褪色,故A错误;
B.乙烯中含双键,能与溴水发生加成反应使溴水褪色,故B正确;
C.苯环为平面结构,则苯分子中所有原子均在同一平面上,故C正确;
D.乙醇中含-OH,在浓硫酸作用下可与乙酸发生酯化反应,属于取代反应,故D正确;
故选A.
A.甲烷为饱和烃,与高锰酸钾不反应,则不能使酸性高锰酸钾溶液褪色,故A错误;
B.乙烯中含双键,能与溴水发生加成反应使溴水褪色,故B正确;
C.苯环为平面结构,则苯分子中所有原子均在同一平面上,故C正确;
D.乙醇中含-OH,在浓硫酸作用下可与乙酸发生酯化反应,属于取代反应,故D正确;
故选A.
点评:本题考查有机物的结构与性质,为高频考点,把握常见有机物的比例模型、官能团与性质的关系为解答的关键,侧重有机物性质、空间结构的考查,题目难度不大.

练习册系列答案
相关题目
根据下列反应判断有关物质的还原性由强到弱的顺序正确的是( )
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
①H2SO3+I2+H2O═2HI+H2SO4
②2FeCl3+2HI═2FeCl2+2HCl+I2
③3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A、H2SO3>I->Fe2+>NO |
| B、I->H2SO3>Fe2+>NO |
| C、Fe2+>I->H2SO3>NO |
| D、NO>Fe2+>H2SO3>I- |
下列说法正确的是( )
| A、铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B、设想把“H2+Cl2═2HCl”设计成燃料电池,用于工业制盐酸,并进行发电 |
| C、纯锌与稀硫酸反应产生氢气的速率较慢,再加入少量CuSO4固体,速率不变 |
| D、原电池的两极一定是由活泼性不同的两种金属组成 |
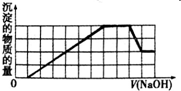 某溶液中可能含有H+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示.下列说法正确的是( )
某溶液中可能含有H+、NH4+、Fe3+、Al3+、SO42-、CO32-等离子.当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化的图象如图所示.下列说法正确的是( )| A、原溶液中含有的阳离子只有H+、Fe3+、Al3+ |
| B、原溶液中一定含有SO42-和Na+ |
| C、原溶液中含有的Fe3+和Al3+的物质的量之比为l:l |
| D、反应最后形成的溶液中溶质只有Na2SO4 |
下列4个化学反应,与其他3个反应类型不同的是( )
A、CH2═CH-CH3+HCl
| |||
B、CH3CHO+H2
| |||
C、CH3CH2Br+NaOH
| |||
| D、CH≡CH+2Br2-→CH Br2CH Br2 |
 )的单体.某课题组用有机物A(分子式C4H9Br,分子中有3个甲基)和甲醇为有机原料合成H.合成路线如下:
)的单体.某课题组用有机物A(分子式C4H9Br,分子中有3个甲基)和甲醇为有机原料合成H.合成路线如下: