题目内容
10.实验室可以用KMnO4标准液滴定草酸(H2C2O4),测定溶液中草酸的浓度.判断下列说法不正确的是( )| A. | 滴定中涉及的离子方程式为:2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O | |
| B. | KMnO4标准溶液常用硫酸酸化,若用HNO3酸化,会使测定结果偏低 | |
| C. | KMnO4标准溶液盛放在酸式滴定管中 | |
| D. | 该实验选择酚酞做指示剂,当待测液颜色由无色变为浅红色时即达到滴定终点 |
分析 用KMnO4标准液滴定草酸(H2C2O4),发生氧化还原反应,高锰酸钾具有强氧化性,可氧化腐蚀橡胶,且为紫色,该滴定实验不需要指示剂,以此来解答.
解答 解:A.Mn得到电子,C失去电子,由电子、电荷守恒可知,离子反应为2MnO4-+5H2C2O4+6H+═2Mn2++10CO2↑+8H2O,故A正确;
B.硝酸具有强氧化性,可与草酸反应,消耗高锰酸钾减少,则KMnO4标准溶液常用硫酸酸化,若用HNO3酸化,会使测定结果偏低,故B正确;
C.高锰酸钾具有强氧化性,可氧化腐蚀橡胶,则KMnO4标准溶液盛放在酸式滴定管中,故C正确;
D.高锰酸钾溶液为紫色,不需要加指示剂,滴定终点时由无色变为紫色,且半分钟内不变色,故D错误;
故选D.
点评 本题考查中和滴定实验及氧化还原反应,为基础性习题,把握氧化还原反应的应用、实验操作及试剂的颜色为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
1.常温下,向2L恒容密闭容器中冲入1.0molM和1.0molN,发生如下反应:M(g)+N(g)?P(g).一段时间后达到平衡.反应过程中测定的部分数据见下表,下列说法正确的是( )
| t/s | 0 | 5 | 15 | 25 | 35 |
| N(M)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
| A. | 35s时,N的浓度为0.80mol•L-1 | |
| B. | 达到平衡时,M的转化率为80% | |
| C. | 相同温度下若起始时向容器中充入1.0molP,则达到平衡时P的浓度为0.1mol•L-1 | |
| D. | 相同温度下,起始时向容器中充入0.20molM、0.20molN和1.0molP,反应达到平衡前v(逆)<v(正) |
18.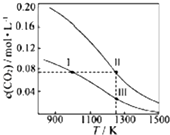 在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
 在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )| A. | 反应CO2(g)+C(s)?2CO(g)的△S>0、△H<0 | |
| B. | 体系的总压强P总:P总(状态Ⅱ)<2P总(状态Ⅰ) | |
| C. | 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) | |
| D. | 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ) |
5.用四种溶液进行实验,下表中“操作及现象“与”溶液“对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入二氧化碳,溶液变浑浊 | 饱和碳酸钠溶液 |
| B | 通入二氧化碳,溶液变浑浊,继续通二氧化碳至过量,浑浊消失 | 硅酸钠溶液 |
| C | 通入二氧化碳,溶液变浑浊,继续通二氧化碳至过量,浑浊消失,再加入足量氢氧化钠溶液,又变浑浊 | 澄清石灰水 |
| D | 通入二氧化碳,溶液变浑浊,再加入品红溶液,红色褪色 | 次氯酸钙溶液 |
| A. | A | B. | B | C. | C | D. | D |
15.下列各物质投入水中,使溶液呈酸性的是( )
| A. | NaOH | B. | NH3 | C. | CH3COONa | D. | NH4Cl |
19.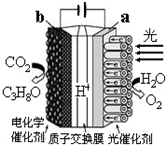 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和C3H8O.下列说法错误的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和C3H8O.下列说法错误的是( )
 某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和C3H8O.下列说法错误的是( )
某模拟“人工树叶”电化学实验装置如图所示,该装置能将H2O和CO2转化为O2和C3H8O.下列说法错误的是( )| A. | 该装置将光能和电能转化为化学能 | |
| B. | 该装置工作时,H+从a极区向b极区迁移 | |
| C. | 每还原44 g CO2,理论上可生成33.6L O2 | |
| D. | b电极的反应为:3CO2+18H++18e-═C3H8O+5H2O |
20.高铁酸钠(Na2FeO4)是一种高效多功能水处理剂.工业上通过以下反应生产:
3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4+3NaCl+6NaNO3+5H2O
下列有关该反应的说法正确的是( )
3NaClO+2Fe(NO3)3+10NaOH═2Na2FeO4+3NaCl+6NaNO3+5H2O
下列有关该反应的说法正确的是( )
| A. | 氯元素的化合价升高 | B. | Fe(NO3)3是氧化剂 | ||
| C. | 铁元素被氧化 | D. | NaOH发生氧化反应 |
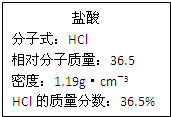 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题: