题目内容
15.某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+.取该溶液100mL,加入过量NaOH溶液并加热,得到0.02mol气体,同时产生红褐色沉淀;将过滤洗涤后的沉淀灼烧得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀.下列说法正确的是( )| A. | 该溶液中最多存在4种离子 | |
| B. | 该溶液可由KCl、(NH4)2SO4和FeCl3配制而成 | |
| C. | 该溶液中一定存在Cl-、且c(Cl-)≥0.4mol•L-1 | |
| D. | 该溶液中不能确定是否存在CO32- |
分析 取该溶液100mL,加入过量NaOH溶液并加热,得到0.02mol气体,则一定含0.02molNH4+,同时产生红褐色沉淀;将过滤洗涤后的沉淀灼烧得到1.6g固体,为氧化铁,其物质的量为$\frac{1.6g}{160g/mol}$=0.01mol,则原溶液中一定含0.02molFe3+;因Fe3+、CO32-不能共存,则一定不含CO32-;
向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀,白色沉淀为硫酸钡,物质的量为$\frac{4.66g}{233g/mol}$=0.02mol,则原溶液一定含0.02molSO42-,结合电荷守恒来解答.
解答 解:由上述分析可知,一定含SO42-、NH4+、Fe3+,一定不含CO32-,由电荷守恒可知0.02mol×1+0.02mol×3>0.02mol×2,则一定还含阴离子Cl-,不能确定是否含K+,
A.该溶液中最多存在5种离子,至少存在4种离子,故A错误;
B.若存在(NH4)2SO4,铵根离子与硫酸根离子的物质的量比为2:1,由分析可知二者物质的量比为1:1,故B错误;
C.由电荷守恒可知,该溶液中一定存在Cl-、且c(Cl-)≥$\frac{(0.08-0.04)mol}{0.1L}$=0.4mol•L-1,故C正确;
D.溶液中一定不存在CO32-,故D错误;
故选C.
点评 本题考查常见离子的检验,为高频考点,把握离子之间的反应、离子检验、电荷守恒为解答的关键,侧重分析与推断能力的考查,注意铁离子与碳酸根离子不能共存,题目难度不大.

练习册系列答案
相关题目
5.下列说法正确的是( )
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 溶液中溶质粒子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 | |
| C. | 浓氨水中滴加饱和FeCl3溶液可制得氢氧化铁胶体 | |
| D. | 胶体不一定是液态,胶体的丁达尔效应属于物理变化 |
10.下列仪器及其名称不正确的是( )
| A. |  量筒 | B. |  试管 | C. |  坩埚 | D. |  试剂瓶 |
7.下列物质的分类正确的是( )
| A. | 氧化物:CO2、NO、SO2、H2O | |
| B. | 碱:NaOH、KOH、Ba(OH)2、Na2CO3 | |
| C. | 铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3•H2O | |
| D. | 碱性氧化物:Na2O、CaO、Mn2O7、Fe2O3 |
4.下列说法不正确的是( )
| A. | 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 | |
| B. | 非金属氧化物不一定是酸性氧化物,金属氧化物多数是碱性氧化物 | |
| C. | 同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不同 | |
| D. | 将SO2气体通入BaCl2溶液中至饱和未见沉淀生成,继续通入NO2则有沉淀生成 |
5.分子式为C4H10O的醇与分子式为C4H8O2的羧酸发生酯化反应,生成酯的结构可能有(不考虑立体异构)( )
| A. | 4 种 | B. | 6 种 | C. | 8 种 | D. | 10 种 |
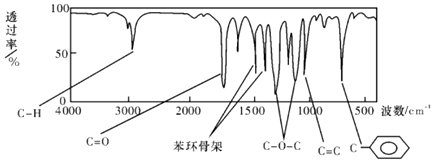
 (不考虑立体异构)
(不考虑立体异构)
 .
.