题目内容
1.0.01mol某液态烷烃完全燃烧需要消耗2.56g氧气,通过计算求该烷烃的化学式.写出全部符合该化学式的烃的结构简式.分析 设烷烃的化学式为CnH2n+2,根据燃烧方程式计算,燃烧方程式为:CnH2n+2+(n+$\frac{2n+2}{4}$)O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O.
解答 解:n(O2)=$\frac{2.56g}{32g/mol}$=0.08mol,
设烷烃的化学式为CnH2n+2,
CnH2n+2+(n+$\frac{2n+2}{4}$)O2$\stackrel{点燃}{→}$nCO2+(n+1)H2O
1 (n+$\frac{2n+2}{4}$)
0.01 0.08
则有:n+$\frac{2n+2}{4}$=$\frac{0.08}{0.01}$=8,解得n=5,故烷烃化学式为:C5H12.结构简式有三种:CH3CH2CH2CH2CH3、(CH3)2CHCH2CH3、(CH3)2C(CH3)2.
答:烷烃分子式为CnH2n+2;结构简式为CH3CH2CH2CH2CH3、(CH3)2CHCH2CH3、(CH3)2C(CH3)2.
点评 本题考查有机物分子式的确定,为高频考点,侧重于学生的分析、计算能力的考查,题目难度不大,注意从有机物燃烧的化学方程式的角度解答该题.

练习册系列答案
相关题目
8.化学与我们的生活密切相关,但我们在改善自己生活环境的同时也破坏了自然,旨在限制温室气体排放量、抵制全球范围内气候持续变暖的《京都议定书》于2005年2月16日正式生效.我国二氧化碳的排放量位居世界第二,下列减少二氧化碳这种温室气体排放的措施不切实际的是( )
| A. | 积极开发氢能源 | B. | 充分利用太阳能 | C. | 不使用化石燃料 | D. | 积极开发核能源 |
6.下列有关溶液组成的描述合理的是( )
| A. | 无色溶液中可能大量存在Al3+、NH4+、Cl?、S2? | |
| B. | 酸性溶液中可能大量存在Fe3+、K+、Cl?、SO42? | |
| C. | 弱碱性溶液中可能大量存在Na+、K+、Cl?、HCO3? | |
| D. | 酸性溶液中可能大量存在Na+、ClO?、SO42?、I? |
11.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染.下列做法不符合绿色化学理念的是( )
| A. | 研制水溶剂涂料替代有机溶剂涂料 | |
| B. | 用可降解塑料生产包装盒或快餐盒 | |
| C. | 用反应:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O 制备硫酸铜 | |
| D. | 用反应:2CH2=CH2+O2$\stackrel{Ag}{→}$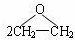 制备环氧乙烷 制备环氧乙烷 |
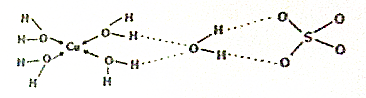
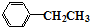 $\stackrel{KMnO_{4}溶液}{→}$
$\stackrel{KMnO_{4}溶液}{→}$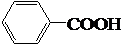
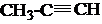 +Br2→CH3-CBr=CHBr
+Br2→CH3-CBr=CHBr $→_{Cl_{2}}^{光照}$
$→_{Cl_{2}}^{光照}$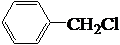 (一卤代物)
(一卤代物)
 、
、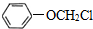 (写两种)
(写两种)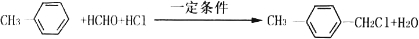 ,
,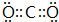 ;一种由E、D组成的化合物与AD2互为等电子体,其化学式为N2O.
;一种由E、D组成的化合物与AD2互为等电子体,其化学式为N2O.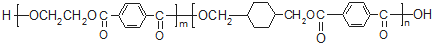
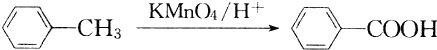
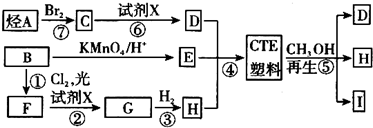
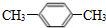 ,I的结构简式为
,I的结构简式为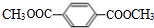 .
.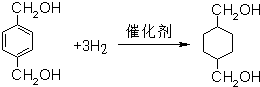 .
.