题目内容
碱式碳酸铜[Cu2(OH)2C03]是一种用途广泛的化工原料.工业上可用电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)制备,其制备过程如下:
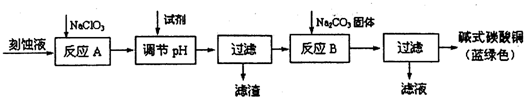
查阅资料知,通过调节溶液的酸碱性可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
(1)氯酸钠的作用是 ;
(2)调节溶液A的pH范围为 ,可以选择的试剂是 .(填序号).
a.氨水 b.硫酸铜 c.氢氧化铜 d.碳酸铜
(3)反应B的温度要控制在60℃左右,且保持恒温,可采用的加热方法是 ;若温度过高,所得蓝绿色沉淀中会有黑色固体出现,黑色固体可能是 .
(4)已知滤液中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式: .
(5)过滤得到的产品洗涤时,如何判断产品已经洗净 .

查阅资料知,通过调节溶液的酸碱性可使Cu2+、Fe2+、Fe3+生成沉淀的pH如下:
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1,4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
(2)调节溶液A的pH范围为
a.氨水 b.硫酸铜 c.氢氧化铜 d.碳酸铜
(3)反应B的温度要控制在60℃左右,且保持恒温,可采用的加热方法是
(4)已知滤液中含有碳酸氢钠,写出生成碱式碳酸铜的离子方程式:
(5)过滤得到的产品洗涤时,如何判断产品已经洗净
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)加具有氧化性的物质氯酸钠,把亚铁离子氧化物铁离子,加入CuO(或氢氧化铜、碳酸铜等)调节pH是铁离子转化为氢氧化铁沉淀,过滤除去沉淀,在滤液中加碳酸钠,生成碱式碳酸铜,过滤得到碱式碳酸铜固体;
(1)根据表中数据可知铁离子容易转化为沉淀,则要把亚铁离子转化为铁离子;
(2)调节溶液A的pH使铁离子转化为沉淀,而铜离子不沉淀;加入的试剂能消耗氢离子,但是不能引入新的杂质;
(3)反应温度较低,应该用水浴加热;碱式碳酸铜受热易分解生成CuO;
(4)氯化铜与碳酸钠反应生成碱式碳酸铜和碳酸氢钠;
(5)检验洗涤是否干净,设计实验检验滤液中是否含有氯离子证明是否洗涤干净.
(1)根据表中数据可知铁离子容易转化为沉淀,则要把亚铁离子转化为铁离子;
(2)调节溶液A的pH使铁离子转化为沉淀,而铜离子不沉淀;加入的试剂能消耗氢离子,但是不能引入新的杂质;
(3)反应温度较低,应该用水浴加热;碱式碳酸铜受热易分解生成CuO;
(4)氯化铜与碳酸钠反应生成碱式碳酸铜和碳酸氢钠;
(5)检验洗涤是否干净,设计实验检验滤液中是否含有氯离子证明是否洗涤干净.
解答:
解:电子工业中刻蚀线路板的酸性废液(主要成分有FeCl3、CuCl2、FeCl2)加具有氧化性的物质氯酸钠,把亚铁离子氧化物铁离子,加入CuO(或氢氧化铜、碳酸铜等)调节pH是铁离子转化为氢氧化铁沉淀,过滤除去沉淀,在滤液中加碳酸钠,生成碱式碳酸铜,过滤得到碱式碳酸铜固体;
(1)根据表中数据可知铁离子在pH=3.7时,即可完全沉淀,则容易转化为沉淀除去,所以要加入氧化剂氯酸钾把亚铁离子氧化为铁离子;
故答案为:将Fe2+氧化成Fe3+并最终除去;
(2)调节溶液A的pH使铁离子转化为沉淀,而铜离子不沉淀,则调节溶液A的pH范围为3.7-6.0;调节pH时,加入的试剂能消耗氢离子,但是不能引入新的杂质,则可以选用氢氧化铜 和碳酸铜;
故答案为:3.7-6.0;cd;
(3)反应B的温度要控制在60℃左右,且保持恒温,由于反应温度较低,则可采用水浴加热的方法;碱式碳酸铜受热易分解生成CuO,所以若温度过高,所得蓝绿色沉淀中会有黑色固体CuO;
故答案为:水浴加热;CuO;
(4)氯化铜与碳酸钠反应生成碱式碳酸铜和碳酸氢钠,其反应的离子方程式为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-;
故答案为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-;
(5)沉淀表面会附着氯离子,设计实验检验是否含有氯离子的方法可以检验是否洗涤干净,实验设计为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净,
故答案为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
(1)根据表中数据可知铁离子在pH=3.7时,即可完全沉淀,则容易转化为沉淀除去,所以要加入氧化剂氯酸钾把亚铁离子氧化为铁离子;
故答案为:将Fe2+氧化成Fe3+并最终除去;
(2)调节溶液A的pH使铁离子转化为沉淀,而铜离子不沉淀,则调节溶液A的pH范围为3.7-6.0;调节pH时,加入的试剂能消耗氢离子,但是不能引入新的杂质,则可以选用氢氧化铜 和碳酸铜;
故答案为:3.7-6.0;cd;
(3)反应B的温度要控制在60℃左右,且保持恒温,由于反应温度较低,则可采用水浴加热的方法;碱式碳酸铜受热易分解生成CuO,所以若温度过高,所得蓝绿色沉淀中会有黑色固体CuO;
故答案为:水浴加热;CuO;
(4)氯化铜与碳酸钠反应生成碱式碳酸铜和碳酸氢钠,其反应的离子方程式为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-;
故答案为:2Cu2++3CO32-+2H2O=Cu2(OH)2CO3+2HCO3-;
(5)沉淀表面会附着氯离子,设计实验检验是否含有氯离子的方法可以检验是否洗涤干净,实验设计为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净,
故答案为:取最后一次洗涤液,加入硝酸银、稀硝酸,无沉淀生成则表明已洗涤干净.
点评:本题考查了实验探究物质分离方法和物质性质的分析判断,注意把握一些重要的实验操作,掌握物质性质是关键,题目难度中等.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
以下各组离子在该溶液中能大量共存的有( )
| A、滴加石蕊试液显红色的溶液:Fe3+、NH4+、CO32-、I- |
| B、pH值为1的溶液:Cu2+、Na+、Mg2+、NO3- |
| C、水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Cl-、Ba2+ |
| D、所含溶质为Na2CO3的溶液:K+、Na+、NO3-、Al3+ |
对已经达到化学平衡的反应:COCl2(g)?CO(g)+Cl2(g),△H>0 当反应达到平衡时下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减小压强 ⑤加催化剂,其中能提高COCl2(g)转化率的是( )
| A、①⑤ | B、①④ | C、②③ | D、③⑤ |
下列实验装置或操作与粒子的大小有直接关系的是( )
A、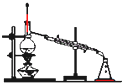 蒸馏 |
B、 蒸发 |
C、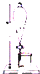 萃取 |
D、 丁达尔效应 |