题目内容
已知常温下FeS的Ksp=6.25×10-18.
(1)常温下FeS的溶解度为多少g?(设饱和溶液的密度为1g?cm-3)
(2)在常温下将过量的FeS投入到0.10mol?L-1的 Na2S溶液中,则平衡时c(Fe2+)为多少?
(1)常温下FeS的溶解度为多少g?(设饱和溶液的密度为1g?cm-3)
(2)在常温下将过量的FeS投入到0.10mol?L-1的 Na2S溶液中,则平衡时c(Fe2+)为多少?
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)溶解度的概念是:某温度下,100g水中所能溶解溶质的质量,据此计算即可;
(2)依据溶度积常数计算即可.
(2)依据溶度积常数计算即可.
解答:
解:(1)FeS饱和溶液中:c(S2-)=c(Fe2+)=2.5×10-9mol/L,溶解度=88g/mol×2.5×10-9mol/L=2.2×10-7g/L=2.2×10-6g/100g,
答:常温下FeS的溶解度为2.2×10-6g;
(2)c(Fe2+)=
=
=6.25×10-17mol/L,答:平衡时c(Fe2+)为6.25×10-17mol/L.
答:常温下FeS的溶解度为2.2×10-6g;
(2)c(Fe2+)=
| Ksp |
| c(S2-) |
| 6.25×10-18 |
| 0.1 |
点评:本题主要考查的是物质溶解度的计算依旧溶度积常数在计算中的应用,难度不大.

练习册系列答案
相关题目
下列事实不能用平衡移动原理解释的是( )
| A、2SO2+O2?2SO3的平衡体系中,加入由18O构成的氧气,则SO2中的18O的含量会增加 | ||||||
B、 I2(g)+H2(g)?2HI(g)加压后颜色加深 I2(g)+H2(g)?2HI(g)加压后颜色加深 | ||||||
C、
| ||||||
D、
|
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0在恒容的密闭容器中,下列有关说法正确的是( )
| 180℃ |
| 催化剂 |
| A、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B、平衡时,其他条件不变,增加NH3的浓度,废气中氮氧化物的转化率减小 |
| C、单位时间内消耗NO和N2的物质的量比为1:2时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
以0.10mol/L的氢氧化钠溶液滴定某一元弱酸的滴定曲线如图所示.横轴为加入氢氧化钠的体积数,纵轴为溶液的pH.下列正确的是( )


| A、此一元弱酸的电离常数(Ka)约为1.0×10-6 |
| B、此弱酸的浓度为1×10-4mol/L |
| C、此实验最好选用甲基红(变色范围在4.2~6.3)作指示剂 |
| D、此滴定反应为吸热反应 |
将W克氯化钠与碳酸氢钠的混合物溶于水,加入足量的氢氧化钡溶液充分反应过滤,称得W克沉淀物.则原混合中氯化钠的质量分数是( )
| A、28.6% |
| B、42.6% |
| C、41.2% |
| D、57.4% |
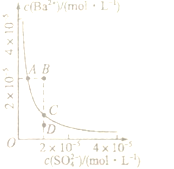 某温度下,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
某温度下,BaSO4在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A、加入Na2SO4可以使溶液由A点变到B点 |
| B、通过蒸发可以使溶液由D点变到C点 |
| C、D点无BaSO4沉淀生成 |
| D、A点对应的Ksp等于c点对应的Ksp |

