题目内容
17.将一定量的碳酸钠和碳酸氢钠的混合物27.4g,跟含溶质0.4mol 的盐酸恰好反应,生成二氧化碳气体.(已知碳酸氢钠和盐酸反应的方程式如下:NaHCO3+HCl→NaCl+CO2↑+H2O )
(1)写出碳酸钠与盐酸反应的化学方程式
(2)求原混合物中碳酸钠和碳酸氢钠的质量各多少克?
(3)求生成的二氧化碳气体在标准状况下的体积.
分析 (1)碳酸钠与盐酸反应生成氯化钠、二氧化碳气体和水;
(2)设出混合物中含有碳酸钠、碳酸氢钠的物质的量,然后分别根据总质量、消耗氯化氢的物质的量列式计算;
(3)根据碳原子守恒计算出生成二氧化碳的物质的量,然后根据V=nVm计算出生成二氧化碳的体积.
解答 解:(1)碳酸钠与盐酸反应生成氯化钠、二氧化碳和水,反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O,
答:碳酸钠与盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O;
(2)设原混合物中含有碳酸钠、碳酸氢钠的物质的量分别为x、y,
则$\left\{\begin{array}{l}{106x+84y=27.4}\\{2x+y=0.4}\end{array}\right.$,
解得:$\left\{\begin{array}{l}{x=0.1mol}\\{y=0.2mol}\end{array}\right.$,
原混合物中含有碳酸钠的质量为:106g/mol×0.1mol=10.6g,含有碳酸氢钠的质量为:84g/mol×0.02mol=16.8g,
答:原混合物中含有碳酸Na2CO3的质量为10.6g,NaHCO3为16.8g;
(3)碳酸钠、碳酸氢钠与盐酸反应生成二氧化碳气体,根据C原子守恒可知生成二氧化碳的物质的量为:0.1mol+0.2mol=0.3mol,
标准状况下0.3mol二氧化碳的体积为:22.4L/mol×0.3mol=6.72L,
答:生成二氧化碳在标准状况下的体积为6.72L.
点评 本题考查了混合物反应的计算,题目难度中等,明确发生反应的原理为解答关键,注意掌握守恒法在化学计算中的应用,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.仪器名称为“分液漏斗”的是( )
| A. | 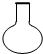 | B. | 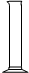 | C. |  | D. |  |
8.下列反应中生成物总能量高于反应物总能量的是( )
| A. | 氧化钙溶于水 | B. | 铁粉与硫粉共热 | C. | 强酸强碱中和 | D. | 碳酸钙分解 |
5.下列关于铝的叙述中,正确的是( )
| A. | 铝是地壳中含量最多的元素 | |
| B. | 常温下,铝能与NaCl溶液发生置换反应 | |
| C. | 铝能溶解于冷浓硝酸中,生成硝酸铝 | |
| D. | 在化学反应中,铝容易失去电子,是还原剂 |
12.在标准状况下,一氧化碳和二氧化碳的混合气体5.6L,如果一氧化碳的质量为5.6g,则二氧化碳的质量为( )
| A. | 5.6g | B. | 4.4g | C. | 2.2g | D. | 1g |
9.做焰色反应实验用的铂丝,每试验一种样品后都必须进行的操作是( )
| A. | 用水洗涤2~3次后再使用 | |
| B. | 用滤纸擦干后才可使用 | |
| C. | 用盐酸洗涤后,经蒸馏水冲洗,方可使用 | |
| D. | 用盐酸洗涤后,再在酒精灯火焰上灼烧到没有颜色,才可使用 |
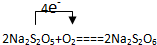 ;
; .
.