题目内容
5.配离子[Mn(CN)6]4-的中心原子为Mn,配位原子为N.分析 配离子[Mn(CN)6]4-中Mn2+离子提供空轨道,N原子提供孤对电子,形成配位键,以此来解答.
解答 解:该配离子中配位体是CN-,Mn2+离子提供空轨道,N原子提供孤对电子,形成配位键,则中心原子为Mn,配位原子为N,
故答案为:Mn;N.
点评 本题考查配位键的形成,为高频考点,把握配位键的形成及中心原子为解答本题的关键,侧重分析与应用的考查,注意原子结构与性质的应用,题目难度不大.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
16.常温下,关于pH=10的氨水和氢氧化钠溶液,下列说法正确的是( )
| A. | n(NH3•H2O)>n(NaOH) | |
| B. | 在氢氧化钠溶液中,c(OH)=1010mol/L | |
| C. | 在氨水中,c(OH)=c(NH4)+c(H) | |
| D. | 0.1mol/L的盐酸分别与等体积的氨水和氢氧化钠溶液恰好完全反应,氨水消耗的盐酸体积少 |
13.5.6g铁粉投入到足量的100mL 2mol/L的稀硫酸中,2min时铁粉刚好溶解,下列表示这个反应的速率正确的是( )
| A. | v(H2SO4)=0.5 mol/(L•min) | B. | v(H2SO4)=1 mol/(L•min) | ||
| C. | v(H+)=0.5 mol/(L•min) | D. | v(FeSO4)=0.5 mol/(L•min) |
20.用如图所示的装置电解KBr溶液制取KBrO3,生成16.7g KBrO3时理论上转移电子的物质的量为( )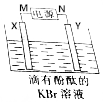

| A. | 0.1mol | B. | 0.2mol | C. | 0.4mol | D. | 0.6mol |
10.将下列物质分别加入到溴水中,溴单质的物质的量减少的是( )
| A. | CCl4 | B. | KI | C. | KCl | D. | Cl2 |
17.120℃时,将H2、C2H5OH、O2的混合气体通入盛有足量Na2O2的密闭容器中,用电火花不断点燃,反应完全后,体系内压强为零,则混合气体中,H2、C2H5OH、O2的物质的量之比可能是( )
| A. | 3:4:1 | B. | 3:1:2 | C. | 7:2:1 | D. | 9:3:1 |
14.室温条件下,下列有关电解质溶液的描述正确是( )
| A. | 向Na2CO3溶液中通入CO2至溶液为中性,则$\frac{c({{N}_{a}}^{+})}{2c(C{{O}_{3}}^{2-})}$>1 | |
| B. | pH相同的氨水和Ba(OH)2溶液中2c(NH4+)=c(Ba2+) | |
| C. | 将CH3COONa溶液从25℃升温至40℃,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$增大 | |
| D. | 向Mg(OH)2浊液中加入少量NH4Cl粉末,$\frac{c(M{g}^{2+})}{c(O{H}^{-})}$不变 |
18.关于CCl4说法错误的是( )
| A. | 晶体类型:分子晶体 | B. | 正四面体结构的分子 | ||
| C. | 含极性键的非极性分子 | D. | 与CH4结构相似、性质相似 |