题目内容
18.在酸性溶液中,能大量共存的离子是( )| A. | Mg2+、Fe3+、NO3-、SCN- | B. | Al3+、Fe2+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、HCO3- | D. | Na+、CH3COO-、NO3-、SO42- |
分析 酸性溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,不能结合生成络离子等,则离子大量共存,以此来解答.
解答 解:A.Fe3+、SCN-结合生成络离子,不能大量共存,故A错误;
B.酸溶液中该组离子之间不反应,可大量共存,故B正确;
C.酸溶液中不能大量存在HCO3-,故C错误;
D.酸溶液中不能大量存在CH3COO-,故D错误;
故选B.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、络合反应的离子共存考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.当光束通过下列分散系①有尘埃的空气②稀硫酸③蒸馏水④墨水⑤Fe(OH)3胶体,能观察到丁达尔效应的有( )
| A. | ①② | B. | ①④⑤ | C. | ②③④ | D. | ②⑤ |
9.设NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 在常温常压下,11.2L N2含有的分子数为0.5NA | |
| B. | 在常温常压下,1mol 氖气含有的原子数为2NA | |
| C. | 27g Al与足量的盐酸反应失去的电子数为3NA | |
| D. | 在同温同压时,相同体积的任何气体单质所含的原子数一定相同 |
6.实验室中保存金属钠的方法是( )
| A. | 放在水中 | B. | 放在四氯化碳中 | C. | 放在石蜡油中 | D. | 放在细沙中 |
13.科学家提出可以用酸度(AG) 表示溶液的酸碱性,AG=lg$\frac{c{(H}^{+})}{c({OH}^{-})}$,下列叙述正确的是( )
| A. | 中性溶液的AG=1 | |
| B. | 常温下0.1 mol•L-1NaOH溶液的AG=12 | |
| C. | 酸性溶液的AG<0 | |
| D. | 常温下0.1 mol•L-1盐酸溶液的AG=12 |
3.下列事实不能用平衡移动原理解释的是( )
| A. | 由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 | |
| B. | 用加热蒸干AlCl3溶液的方法不能制得无水AlCl3 | |
| C. | 蒸馏水和0.1mol•L-1 NaOH溶液中的c(H+),前者大于后者 | |
| D. | 向含有少量Fe3+的MgCl2酸性溶液中加MgCO3,可将Fe3+转化成Fe(OH)3除去 |
10.若在加入铝粉能放出氢气的溶液中,分别加入下列各组离子,一定大量共存的是( )
| A. | NH4+、I-、CO32-、Fe3+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、Mg2+、Cl-、Ca2+ | D. | K+、Na+、Cl-、SO42- |
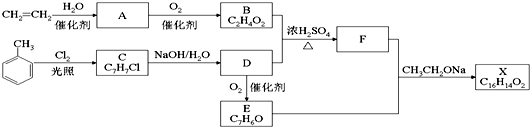
 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$ .B和D反应生成F的化学方程式
.B和D反应生成F的化学方程式 .D→E的化学方程式2
.D→E的化学方程式2 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O. .
. CH2OCH2CH2CHO B.
CH2OCH2CH2CHO B. CH=CHCH2CH2CHO
CH=CHCH2CH2CHO COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.
COOCH2CH2CH3 D.CH2=CHCH=CHCH=CHCH=CHCOOH.