题目内容
 (1)在电化学中,常用碳作电极:
(1)在电化学中,常用碳作电极:①在酸性锌锰干电池中,碳棒作
②若用碳棒和铁棒做电极电解饱和食盐水生产烧碱时,碳棒作
(2)①已知:C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ/mol
则反应CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=
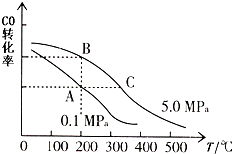
(3)①在一恒容的密闭容器中,由CO和H2合成甲醇:CO(g)+2H2(g)═CH3OH(g)△H.CO的平衡转化率(α)与温度、压强的关系如图所示.A、B两点的平衡常数K(A)
②某温度下,将2.0mol CO和6.0molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25mol/L,请计算出此温度下的平衡常数K值(写出计算过程,计算结果保留二位有效数字).
(4)已知某温度下,Ag2SO4饱和溶液中c(Ag+)=0.04mol/L,则该温度下Ksp(Ag2SO4)=
考点:难溶电解质的溶解平衡及沉淀转化的本质,用盖斯定律进行有关反应热的计算,原电池和电解池的工作原理,化学平衡常数的含义
专题:
分析:(1)锌锰干电池中,碳为正极,电解饱和食盐水时,碳为阳极,发生氧化反应,氯离子被氧化生成氯气;
(2)根据盖斯定律构造出目标反应热化学反应方程式,据此计算反应热;注意化学计量数乘以不同的系数,进行加减,焓变也要乘以相同的系数,做相应加减;
(3)①化学反应的平衡常数随着温度的变化而变化,根据压强恒定,温度变化引起化学平衡移动的方向来判断化学反应的吸放热情况;
②根据化学反应三行式来计算转化率和平衡常数;
(4)根据Ksp(Ag2SO4)=c2(Ag+)c(SO42-)求算.
(2)根据盖斯定律构造出目标反应热化学反应方程式,据此计算反应热;注意化学计量数乘以不同的系数,进行加减,焓变也要乘以相同的系数,做相应加减;
(3)①化学反应的平衡常数随着温度的变化而变化,根据压强恒定,温度变化引起化学平衡移动的方向来判断化学反应的吸放热情况;
②根据化学反应三行式来计算转化率和平衡常数;
(4)根据Ksp(Ag2SO4)=c2(Ag+)c(SO42-)求算.
解答:
解:(1)锌锰干电池中,碳为正极,电解饱和食盐水时,碳为阳极,发生氧化反应,氯离子被氧化生成氯气,反应的电极方程式为2Cl-+2H2O
2OH-+H2↑+Cl2↑,故答案为:正;阳;2Cl-+2H2O
2OH-+H2↑+Cl2↑;
(2)已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol,②C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ/mol,根据盖斯定律,①-②得CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=-393.5-131.3=-524.8kJ/mol,故答案为:-524.8;
(3)①根据图中CO的平衡转化率(α)与温度、压强的关系,A、B两点的温度是一样的,所以平衡常数相等,根据图示内容,压强不变,当温度升该时,一氧化碳的转化率逐渐减小,所以化学平衡向左移动,所以该反应是一个放热反应,故答案为:=;<;
②将2.0mol CO和6.0mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25mol/L,则
CO(g)+2H2(g)═CH3OH(g)
初始浓度:1.0 3.0 0
变化浓度:0.75 1.5 0.75
平衡浓度:0.25 1.5 0.75
此温度下的化学平衡常数K=
=
≈1.3,故答案为:1.3;
(4)Ag2SO4的饱和溶液中,c(Ag+)=4×10-2mol/L,则c(SO42-)=2×10-2mol/L,则Ksp(Ag2SO4)=c2(Ag+)?c(SO42-)=2×10-2×(4×10-2)2=3.2×10-5,故答案为:3.2×10-5.
| ||
| ||
(2)已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol,②C(s)+H2O(g)=CO(g)+H2(g)△H2=+131.3kJ/mol,根据盖斯定律,①-②得CO(g)+H2(g)+O2(g)=H2O(g)+CO2(g),△H=-393.5-131.3=-524.8kJ/mol,故答案为:-524.8;
(3)①根据图中CO的平衡转化率(α)与温度、压强的关系,A、B两点的温度是一样的,所以平衡常数相等,根据图示内容,压强不变,当温度升该时,一氧化碳的转化率逐渐减小,所以化学平衡向左移动,所以该反应是一个放热反应,故答案为:=;<;
②将2.0mol CO和6.0mol H2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.25mol/L,则
CO(g)+2H2(g)═CH3OH(g)
初始浓度:1.0 3.0 0
变化浓度:0.75 1.5 0.75
平衡浓度:0.25 1.5 0.75
此温度下的化学平衡常数K=
| c(CH3OH) |
| c(CO)?c2(H2) |
| 0.75 |
| 0.25×1.52 |
(4)Ag2SO4的饱和溶液中,c(Ag+)=4×10-2mol/L,则c(SO42-)=2×10-2mol/L,则Ksp(Ag2SO4)=c2(Ag+)?c(SO42-)=2×10-2×(4×10-2)2=3.2×10-5,故答案为:3.2×10-5.
点评:本题考查反应热的计算,化学平衡常数、Ksp的计算是现在考试的热点,注意三行式在计算中的应用,题目难度不大,注意盖斯定律的理解与应用.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
对下列流程有关判断正确的是( )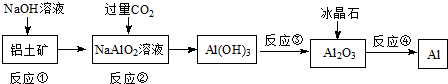

| A、流程中涉及的反应均为非氧化还原反应 |
| B、反应②产生的阴离子主要为CO32- |
| C、实验室中完成反应③应在蒸发皿中进行 |
| D、反应④的条件是电解熔融 |
下列行为不会对环境造成污染的是( )
| A、将生活垃圾就地焚烧 |
| B、大量使用农药以防治病虫害 |
| C、大力提倡使用空调 |
| D、工业废水经处理后循环再用 |
下列的图示与对应的传述相符的是( )
A、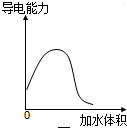 表示稀释冰醋酸过程中溶液导电性的变化曲线 |
B、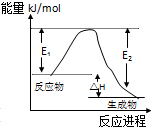 表示某一放热反应,若使用催化剂E1、E2,△H都会发生改变 |
C、 曲线表示将氢氧化钠滴加到醋酸溶液浓度的变化趋势 |
D、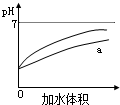 表示pH相同的盐酸与醋酸分别加入水中后溶液pH的变化,其中曲线a对应的是盐酸 |
反应3CO+Fe2O3
2Fe+3CO2可用于工业上炼铁,该反应属于( )
| ||
| A、置换反应 | B、复分解反应 |
| C、化合反应 | D、氧化还原反应 |
工业上可利用反应2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4来制取ClO2,下列关于该反应的说法正确的是( )
| A、SO2发生还原反应 |
| B、NaClO3失去电子 |
| C、H2SO4作氧化剂 |
| D、1mol氧化剂得到1mol电子 |
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、常温常压下,14g N2含有的原子数目为0.5NA |
| B、1mol Na被完全氧化生成Na2O2,失去2NA个电子 |
| C、11.2L O2所含的分子数可能为0.5NA |
| D、0.1mol的Na2O2中含阴离子数是0.2NA |
实验过程中,不会产生气体的( )
A、 |
B、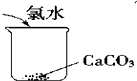 |
C、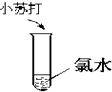 |
D、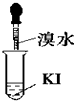 |