题目内容
6.实验室制取乙烯并检验乙烯性质的装置如下图.请回答有关问题: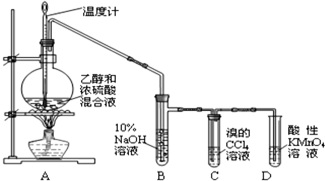
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是防止暴沸.
(2)烧瓶中产生乙烯的反应方程式为
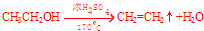 .
.(3)反应开始后,可观察到C和D中共同的现象是褪色; C中的反应类型为加成反应、D中的反应类型为氧化反应.
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是浓硫酸将乙醇和乙酸炭化,浓硫酸被碳还原产生了SO2.
分析 实验室制取乙烯并检验乙烯性质,由实验装置可知,温度计控制温度为170℃时乙醇发生消去反应生成乙烯,B中溶液可吸收乙醇,C中溴的四氯化碳与乙烯发生加成反应,D中乙烯与高锰酸钾发生氧化还原反应,以此来解答.
解答 解:实验室制取乙烯并检验乙烯性质,由实验装置可知,温度计控制温度为170℃时乙醇发生消去反应生成乙烯,B中溶液可吸收乙醇,C中溴的四氯化碳与乙烯发生加成反应,D中乙烯与高锰酸钾发生氧化还原反应,
(1)烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是防止暴沸,故答案为:防止暴沸;
(2)烧瓶中产生乙烯的反应方程式为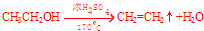 ,故答案为:
,故答案为: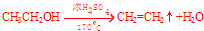 ;
;
(3)反应开始后,可观察到C和D中共同的现象是褪色,C中发生加成反应,而D中发生氧化反应,故答案为:褪色;加成;氧化;
(4)反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是浓硫酸将乙醇和乙酸炭化,浓硫酸被碳还原产生了SO2,
故答案为:浓硫酸将乙醇和乙酸炭化,浓硫酸被碳还原产生了SO2.
点评 本题考查乙烯的制备及性质实验,为高频考点,把握制备原理、实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
相关题目
16.下列分散系中,分散质微粒半径最小的是( )
| A. | 雾 | B. | 蛋白质溶液 | C. | NaCl溶液 | D. | 新制Cu(OH)2悬浊液 |
17.下列物质不属于有机物的是( )
| A. | 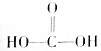 | B. | CO(NH2)2 | C. | CCl4 | D. | 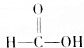 |
14.下列说法正确的是( )
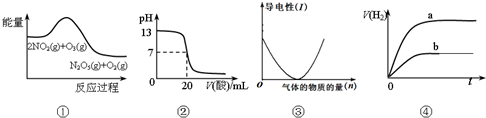

| A. | ①表示化学反应2NO2(g)+O3(g)═N2O5(g)+O2(g)△H>0 | |
| B. | ②表示25℃时,用0.1 mol/LCH3COOH溶液滴定20 mL 0.1 mol/L NaOH溶液,溶液的pH随加入醋酸体积的变化 | |
| C. | ③可表示向醋酸溶液中通入氨气时,溶液导电性随氨气量的变化 | |
| D. | ④表示体积和pH均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 |
1.下列关于普通玻璃的叙述中,正确的是( )
| A. | 玻璃是人类是早使用的硅酸盐材料 | |
| B. | 玻璃在加热熔化时有固定的熔点 | |
| C. | 制普通玻璃的主要原料是纯碱、石灰石、石英 | |
| D. | 普通水泥的成分主要是硅酸钠、硅酸钙和二氧化硅 |
11.乙烯和苯是两种基本化工原料,下列有关说法正确的是( )
| A. | 乙烯和苯都可以从煤焦油中获得 | |
| B. | 乙烯和苯都是平面结构,因为二者分子中都含有碳碳双键 | |
| C. | 乙烯和苯都能使溴水褪色,且褪色的原因相同 | |
| D. | 乙烯和苯都能与H2发生加成反应 |
7.某恒温密闭容器中,可逆反应A(s)?B+C(g)△H=+Q kJ•mol-1(Q>0)达到平衡.缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等.以下分析正确的是( )
| A. | 产物B的状态只能为固态或液态 | |
| B. | 平衡时,单位时间内n(A)消耗﹕n(C)消耗=1﹕1 | |
| C. | 若开始时向容器中加入1molB和1molC,达到平衡时放出热量等于Q kJ | |
| D. | 保持体积不变,向平衡体系中加入A,平衡向正反应方向移动 |