题目内容
等质量的钠、镁、铝分别与足量稀硫酸反应,产生气体的质量比为
- A.1∶2∶3
- B.23∶24∶27
- C.36∶69∶92
- D.23∶12∶9
C
根据化学方程式计算如下:
2Na+H2SO4 Na2SO4+H2↑
Na2SO4+H2↑
46 2
m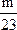
Mg+H2SO4![]() MgSO4+H2↑
MgSO4+H2↑
24 2
m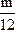
2Al+3H2SO4![]() Al2(SO4)3+3H2↑
Al2(SO4)3+3H2↑
54 6
m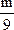
所以生成H2的质量比为![]() ∶
∶![]() ∶
∶![]() =
=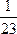 ∶
∶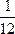 ∶
∶ =36∶69∶92
=36∶69∶92
根据化学方程式计算如下:
2Na+H2SO4
 Na2SO4+H2↑
Na2SO4+H2↑46 2
m
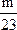
Mg+H2SO4
24 2
m
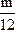
2Al+3H2SO4
54 6
m
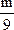
所以生成H2的质量比为
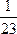 ∶
∶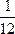 ∶
∶ =36∶69∶92
=36∶69∶92 
练习册系列答案
相关题目
|
金属锂是密度最小的金属,等质量的金属锂能释放出更多的电子,故常用来制造高能量电池.已知锂的金属性介于钠和镁之间,则下列能冶炼出金属锂的方法是 | |
| [ ] | |
A. |
电解法 |
B. |
热还原法 |
C. |
热分解法 |
D. |
铝热法 |
金属锂是密度最小的金属,等质量的金属,锂可以释放出更多的电子,故常用来制造高性能电池。已知锂的金属性介于钠和镁之间,则冶炼金属锂应采用的方法是( )
A.电解法 B.热还原法 C.热分解法 D.铝热法
金属锂是密度最小的金属,等质量的金属锂能释放出更多的电子,故常用来制造高能量电池。已知锂的金属性介于钠和镁之间,则下列能冶炼出金属锂的方法是( )
| A.电解法 | B.热还原法 | C.热分解法 | D.铝热法 |